Um manual para revisão sistemática e meta-análise pré-clinica
Boas vindas!
Olá revisores e revisoras!
Encontre aqui informações, links, artigos e outras ferramentas úteis para te guiar ao longo de uma revisão sistemática.
Navegue pelas seções e saiba mais sobre o que é uma revisão sistemática pré-clínica, quais são os passos e como completá-los.
Use a lista de conteúdos no menu a esquerda da tela para navegar pelos passos de uma revisão sistemática.
Se você tiver questões a respeito do conteúdo ou quiser fazer alguma outra pergunta sobre esse tipo de revisão, envie um Email pra nós CAMARADES BR (em português) ou para CAMARADES Berlin (em inglês).
1 Revisão Sistemática Pré-clínica
Você está pensando em iniciar uma Revisão Sistemática Pré-clínica (RS), e agora?
Continue rolando a página para saber mais sobre o que é uma revisão sistemática pré-clínica, quais são as etapas envolvidas e como conduzi-las.
Use o índice no lado esquerdo, em dispositivos grandes, ou acima da tela em dispositivos menores, para navegar pelas etapas de uma revisão sistemática.
1.1 O que é uma revisão sistemática?
Uma revisão sistemática (RS) é uma revisão de literatura que envolve localizar, avaliar e sintetizar evidências de estudos científicos sistematicamente para responder a uma pergunta de pesquisa definida com base em critérios pré-especificados.
Os métodos de uma revisão sistemática (e meta-análise) devem ser transparentes e reproduzíveis, além de mapeados e relatados para que a revisão possa ser repetida.
1.2 O que é uma meta-análise?
Um método de combinação de resultados quantitativos de estudos individuais identificados por meio de revisão sistemática em uma análise estatística geral.
1.3 Revisões clínicas e pré-clínicas
1.3.1 Pré-clínica
Revisões pré-clínicas tendem a incluir muitos estudos. Os estudos incluídos tendem a ter pequenos tamanhos de amostra e design experimental variado. As revisões pré-clínicas podem ser usadas para:
- Investigar falha translacional
- Explorar diferenças entre estudos (heterogeneidade), por exemplo, validade interna e externa
- Informar futuros estudos pré-clínicos, por exemplo, seleção de modelo
- Informar os ensaios clínicos em fase inicial
- Explicar as discrepâncias nos resultados de ensaios pré-clínicos vs. clínicos
- Informar as decisões dos 3Rs
1.3.2 Clínica
As revisões clínicas tendem a incluir menos estudos, com tamanhos de amostra maiores e a variabilidade entre os estudos incluídos é reduzida com critérios de inclusão mais rigorosos. As revisões clínicas podem ser usadas para:
- Explorar a heterogeneidade, por exemplo, populações clínicas
- Informar estudos clínicos em fase avançada
- Informar a prática clínica e as diretrizes
1.4 Por que realizar RSs pré-clínicas?
- Para resumir evidências de vários estudos semelhantes para permitir estimativas de efeito mais precisas
- Os métodos usados para encontrar e selecionar estudos são transparentes e reproduzíveis, reduzindo o enviesamento e aumentando a probabilidade de produzir conclusões confiáveis e precisas.
- Para resumir as descobertas de todos os estudos disponíveis, tornando as informações mais fáceis para o usuário final ler e entender
- Analisar a qualidade de estudos individuais para apresentar confiança nos resultados
- Síntese quantitativa dos resultados (meta-análise)
- Permitir deduções baseadas em evidências
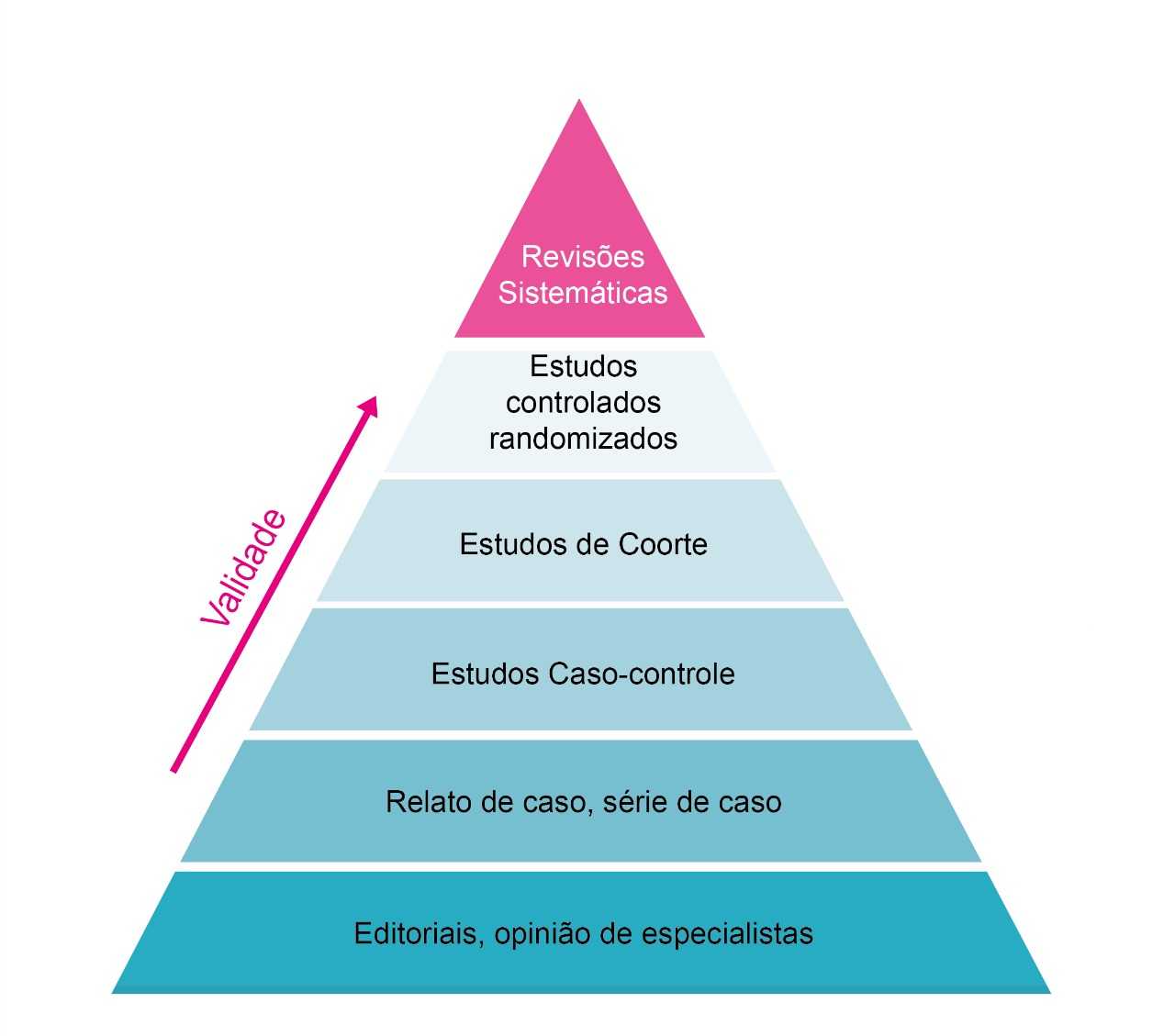
Os resultados de revisões sistemáticas pré-clínicas podem:
- Fornecer evidências para mudar a prática de pesquisa, identificando riscos de enviesamento em experimentos pré-clínicos
- Influenciar o desenvolvimento de diretrizes para relatório de pesquisa e políticas editoriais
- Fornecer evidências para estimular a divulgação de resultados positivos, negativos e neutros por meio da detecção de viés de publicação
- Identificar as características do desenho do estudo que comprometem uma potencial aplicação clínica
- Contribuir para o desenho de ensaios clínicos baseados em evidências
2 Revisões sistemáticas e 3Rs
Os princípios dos 3Rs (Substituição, Redução e Refinamento - Replacement, Reduction, and Refinement, em inglês) são uma abordagem para a pesquisa humanizada com animais. A revisão sistemática é uma ferramenta valiosa para o avanço dos 3Rs, principalmente por meio da redução e refinamento do uso de animais em pesquisas. Usando dados animais existentes, a revisão sistemática pode contribuir para melhorias nos estudos com animais, incluindo:
- Fornecer dados confiáveis para corroborar cálculos de tamanho amostral para vários resultados experimentais
- Permitir a comparação do desempenho estatístico de diferentes medidas de resultados experimentais
- Caracterizar até que ponto submeter animais a múltiplos testes contribui para o conhecimento adicional
- Avaliar se a mesma informação pode ser fornecida através de testes menos invasivos
- Para mais exemplos de revisões sistemáticas que implementam os 3Rs e o bem-estar animal, consulte Ritskes-Hoitinga & van Luijk, 2019.
- E a Diretriz para Relato de Pesquisa Animal: ARRIVE 2.0.
3 Antes de Começar
Há algumas coisas a serem verificadas antes de iniciar sua RS. Leia mais abaixo.
3.1 Ela é necessária?
Considere o seguinte antes de iniciar sua RS:
- A questão tem relevância contemporânea?
- A pergunta tem importância clínica ou importância para informar sobre projetos de experimentos com animais?
- Existe, atualmente, variação na prática?
- Há incerteza e debate na área?
- Informando um design definitivo de experimentos em animais
3.2 Isso já foi feito antes?
Faça uma pesquisa rápida no PubMed ou na base de dados bibliográficos mais usada em sua área para verificar as revisões sistemáticas publicadas. Além disso, verifique os arquivos de pré-publicações, em sites como bioRxiv, medRxiv ou OSF, para ver se uma revisão sistemática foi publicada como uma pré-publicação. Verifique se há revisões sistemáticas em andamento no PROSPERO.
As perguntas a serem feitas sobre as revisões sistemáticas existentes na área incluem:
- A pergunta de pesquisa foi abordada de forma adequada?
- A metodologia da revisão sistemática utilizada na revisão tem qualidade?
- A pergunta de pesquisa é específica ou ampla o suficiente para o seu objetivo?
- Há quanto tempo a revisão sistemática foi realizada?
Não há necessidade de iniciar uma revisão sistemática se uma RS recente, existente e de alta qualidade responder à sua pergunta de pesquisa. Se houver uma RS relevante que não esteja atualizada, considere entrar em contato com a equipe do autor original para discutir seus planos de atualização da revisão ou uma possível colaboração.
Para leitura adicional sobre como avaliar a qualidade de uma revisão sistemática publicada, consulte as diretrizes PRISMA e outras diretrizes apropriadas na página do EQUATOR.
3.3 Existe uma já em andamento?
Antes de começar, verifique se a revisão que você está interessado em conduzir já não está sendo desenvolvida por outro grupo de pesquisa.
Onde posso encontrar esta informação? Verifique os locais onde um protocolo de revisão sistemática pode ser pré-registrado ou publicado, como a PROSPERO, OSF, SyRF, servidores de pré-publicação da sua área, como bioRxiv ou medRxiv. Veja mais abaixo: Registre seu protocolo.
Se você não encontrar nada, vá em frente e inicie sua RS.
Se você descobrir que alguém está trabalhando com uma mesma pergunta de pesquisa ou em uma pergunta semelhante, entre em contato com a equipe. Pergunte sobre seus objetivos, métodos e em que estágio da RS eles estão e se você pode colaborar para alcançar o objetivo comum.
3.4 Construa sua equipe de revisão sistemática
Uma revisão sistemática pode levar muito tempo, portanto, certifique-se de ter a experiência e o financiamento adequados para concluir a revisão. Chame seus colegas para ajudar! E entre em contato com pessoas fora de sua equipe para obter aconselhamento especializado.
Bibliotecários e especialistas em informação podem ajudar a refinar sua estratégia de busca. Eles terão insights sobre quais bancos de dados bibliográficos contêm a literatura sobre as áreas e tópicos de seu interesse. Os bibliotecários podem ajudá-lo a identificar fontes de literatura cinzenta e poderão lhe auxiliar a encontrar versões com o texto integral de artigos que você deseja incluir em sua revisão, especialmente se eles não estiverem disponíveis através da sua assinatura institucional.
Metodologistas de Revisão Sistemática: Se você é novo nos métodos de revisão sistemática, um metodologista poderá ajudá-lo a planejar e organizar sua revisão, recomendar softwares e ferramentas, bem como fornecer suporte para a meta-análise.
Você pode precisar de aconselhamento adicional de um especialista em estatística para a meta-análise, e é bom envolver alguém o mais cedo possível no processo de revisão.
Conhecimento do tópico: Certifique-se de que você tenha em sua equipe pesquisadores e outras partes interessadas com conhecimento adequado do tópico.
Gestão do Projeto: A realização de uma revisão sistemática requer uma gestão eficaz do projeto. Certifique-se de que haja um líder explícito e dedicado que supervisionará o projeto durante todo o processo. O líder do projeto é responsável por manter a visão geral, em qual estágio está a revisão e convidar diferentes membros para a equipe quando necessário. No início do processo de revisão, é necessário decidir uma padronização de nomenclatura para documentos e um local compartilhado para armazenar todos os documentos relacionados à revisão. Pode ser necessário voltar a algum estágio da revisão e rever decisões ou encontrar informações, portanto, tenha um bom controle dos registros. Tome notas detalhadas das decisões tomadas ao longo do processo da RS, quaisquer desvios do protocolo. Essa não é apenas uma prática boa e que aumenta a transparência, mas também pode ajudar a garantir que todos os membros da equipe estejam na mesma página.
4 Pergunta de Pesquisa
O primeiro passo é definir a sua pergunta de pesquisa. Uma pergunta de pesquisa concisa é a base para uma boa estratégia de busca, pois determina a estrutura e a sequência de suas pesquisas na literatura.
As perguntas de pesquisa de RSs pré-clínicas geralmente são centradas em uma intervenção ou exposição e adotam a seguinte estrutura:
População, participantes ou problema: Quais são as características da população ou participantes (espécie, sexo, estágio de desenvolvimento, fatores de risco, ou, para participantes humanos, demografia, condições pré-existentes, etc)? Qual é a condição ou doença de interesse?
Intervenção ou Exposição: Qual é a intervenção ou exposição em consideração para esta população?
Comparação: Qual é a alternativa para a intervenção (por exemplo, placebo, medicamento diferente, cirurgia)?
Resultado/Desfecho: Quais são os resultados relevantes (por exemplo, qualidade de vida, mudança no estado clínico, morbidez, efeitos adversos, complicações)?
Existem outras estruturas de perguntas de pesquisa, dependendo da sua área ou tópico de interesse, por exemplo, revisões de testes diagnósticos e revisões prognósticas. Para obter mais informações, consulte este artigo (em inglês) sobre Como Formular Perguntas de Revisão.
4.1 Partes Interessadas
Envolva as partes interessadas no início da fase de revisão para garantir que a pergunta de pesquisa e as descobertas da revisão sejam relevantes.
Considere o seguinte:
- Quem usará os resultados de sua revisão sistemática?
- Do ponto de vista deles, quais são as perguntas relevantes a serem feitas?
4.2 Exemplos para revisões pré-clínicas
Para referência, veja exemplos de perguntas de pesquisa para revisões publicadas.
"Qual é o efeito dos antidepressivos em comparação com o veículo ou com o não tratamento no volume do infarto em modelos animais de acidente vascular cerebral isquêmico?"
P - Modelos animais de acidente vascular cerebral isquêmico
I - Antidepressivos
C - Veículo ou sem tratamento
R - Volume do infarto
5 Protocolo
O que é um protocolo e por que ter um?
Um protocolo de revisão sistemática descreve porquê e como você conduzirá sua revisão sistemática. Deve incluir sua pergunta de pesquisa, contextualização e os métodos que serão usados, incluindo: estratégia de busca, critérios de inclusão, extração de dados, avaliação de qualidade, síntese de dados e plano de análise estatística.
Ter um protocolo pré-especificado melhora a transparência metodológica de sua revisão sistemática e reduz o risco de enviesamento. A publicação do seu protocolo permite que outras pessoas localizem as revisões em andamento e permite a replicação futura. O processo de montar seu protocolo geralmente envolve a comunicação entre várias partes interessadas importantes, você pode discutir isso com um grupo de aconselhamento, especialistas externos ou seus financiadores.
5.1 Modelos de Protocolo
O SYRCLE (SYStematic Review Centre for Laboratory Animal Experimentation - Centro de Revisão Sistemática para Experimentação com Animais em Laboratório) desenvolveu um modelo de protocolo adaptado para a preparação, registro e publicação de revisões sistemáticas de estudos de intervenção em animais. Veja o modelo e a publicação aqui.
Também pode ser útil olhar exemplos do SyRF Protocol Registry (Registros de Protocolos SyRF) enquanto você formula seu protocolo. Consulte o Registro de Protocolos para verificar se nenhuma revisão sistemática com a mesma pergunta de pesquisa está em andamento no momento.
5.2 Registre seu protocolo
Disponibilizar o protocolo para sua revisão sistemática à comunidade têm vários benefícios: fornece evidências de que análises pré-especificadas foram de fato pré-especificadas; permite que outros comentem sobre sua abordagem; fornece exemplos para outros que planejam tais revisões; e pode ajudá-lo a identificar se outras revisões em áreas semelhantes já estão em andamento. Você pode pesquisar a lista de protocolos por título, data, pessoa responsável ou instituição.
PROSPERO: O Centro de Revisões e Disseminação da Universidade de York agora publica os Protocolos de Revisão Sistemática Pré-clínica. Para mais informações sobre como se registrar no PROSPERO, consulte o site aqui.
OSF: Você pode pré-registrar seu projeto de revisão sistemática no Open Science Framework aqui.
5.3 Seu protocolo e 3RS
Recomendamos que você inclua uma declaração em seu protocolo descrevendo como sua pesquisa afetará os 3Rs (Substituição, Redução e Refinamento) no uso de animais em pesquisa.
6 Busca Sistemática
Para identificar estudos relevantes para incluir em sua RS, você precisa realizar uma pesquisa bibliográfica abrangente com base em uma estratégia de busca bem projetada.
6.1 Selecionando Bases de Dados
Bases de dados:
O primeiro passo é decidir em quais bases de dados pesquisar, isso vai depender da sua área de pesquisa e pergunta de pesquisa. As bases de dados diferem em sua cobertura de periódicos e como os artigos são indexados. Para pesquisas pré-clínicas, bancos de dados típicos incluem PubMed, Embase e Web of Science. Um bibliotecário ou especialista em bases de dados bibliográficos poderá ajudá-lo a identificar outras bases de dados em potencial e construir termos de pesquisa específicos para usar na busca. É uma prática comum pesquisar em várias bases de dados para garantir uma cobertura adequada e eficiente.
Além de bases de dados eletrônicas, você pode usar outros métodos para encontrar artigos relevantes, tais como: escanear listas de referência de estudos relevantes (estudos primários e revisões), pesquisar manualmente os principais periódicos, entrar em contato com especialistas na área e pesquisar outras fontes relevantes na internet. Mantenha um registro dos métodos alternativos usados e os dados coletados em um formato estruturado.
PubMed
PubMed é um banco de dados bibliográfico composto por mais de 30 milhões de citações de literatura biomédica do MEDLINE, periódicos de ciências da vida e livros online.
É um recurso gratuito que apoia a busca e recuperação de literatura biomédica e ciências da vida com o objetivo de melhorar a saúde. É mantido pelo Centro Nacional de Informações sobre Biotecnologia (NCBI) da Biblioteca Nacional de Medicina dos EUA.
Links e recursos: O PubMed Advanced Search Builder é uma ferramenta útil para construir sua consulta de pesquisa.
Informações sobre MeSH Headings.
Embase
O Embase é um banco de dados de pesquisa biomédica que cobre a literatura de 1947 até os dias atuais. Ele contém mais de 32 milhões de registros, incluindo títulos MEDLINE e artigos de 2.900 periódicos exclusivos do Embase.
Você pode acessar o Embase diretamente ou através do Ovid, dependendo da sua assinatura.
Mais informações sobre os arquivos do Embase e o EmTree Headings podem ser encontradas aqui.
Web of Science
Web of Science é uma base de dados de citações independente de editores. A Web of Science Core Collection indexa periódicos acadêmicos, livros e procedimentos nas áreas de ciências, ciências sociais e artes e humanidades e pode ser usada para navegar em toda a rede de citações.
A Web of Science também pode ser usada para pesquisar outras bases de dados, incluindo SciELO, KCI-Korean Journal Database e Zoological Record.
Outras fontes e literatura cinzenta
Outras bases de dados bibliográficos incluem:
- O Cochrane Central Register of Controlled Trials (CENTRAL)
- Google Scholar
- Scopus
- Cumulative Index to Nursing and Allied Health Literature CINAHL
- PsycINFO
O acesso pode variar dependendo do acesso institucional. Documente sua estratégia de busca para que seja suficientemente reproduzível.
6.2 Desenvolvimento de estratégia de busca
Selecione seus termos de pesquisa com base em cada um dos conceitos PICR (ou equivalentes) em sua pergunta de pesquisa.
6.2.1 Etapa 1
Etapa 1: encontre palavras-chave e sinônimos para cada elemento
Um bom exercício é pensar no máximo de sinônimos possível para cada um dos principais conceitos ou elementos PICO.
Por exemplo:
Se sua pergunta de pesquisa for: Qual é o efeito dos antidepressivos em comparação com o veículo ou com o não tratamento no volume do infarto em modelos animais de acidente vascular cerebral?
População: AVC. Sinônimos podem incluir: isquemia cerebral, acidente vascular cerebral.
Intervenção: Antidepressivos. Sinônimos podem incluir: fluoxetina, SSRIs
6.2.2 Etapa 2
Etapa 2: termos de índice/assunto (específicos da base de dados)
Cada base de dados central tem seu próprio sistema de indexação de termos, tópicos e assuntos. Verifique quais os títulos de assunto e termos de indexação presentes nas bases de dados que você está interessado em pesquisar antes de começar.
- Termos MeSH
- Termos Emtree
- (Veja mais informações sobre MeSH e EMTREE acima de Selecionando bases de dados)
Por que usar palavras-chave e termos indexados em sua estratégia de busca?
Os artigos no PubMed são indexados manualmente, mas geralmente há um pequeno atraso. Para capturar todos os artigos que usam linguagem não padrão, incluindo os publicados recentemente, você pode perder alguns usando apenas uma pesquisa por palavra-chave.
6.2.3 Etapa 3
Etapa 3: Combinando termos de busca
Operadores booleanos
O operador OR é usado para conectar dois ou mais conceitos semelhantes (sinônimos). Ele é usado para ampliar os resultados informando ao banco de dados que pelo menos um dos termos de pesquisa deve estar presente nos resultados.
O operador AND é usado para restringir os resultados. Ele é usado para informar ao banco de dados que todos os termos de pesquisa devem estar presentes em cada resultado.
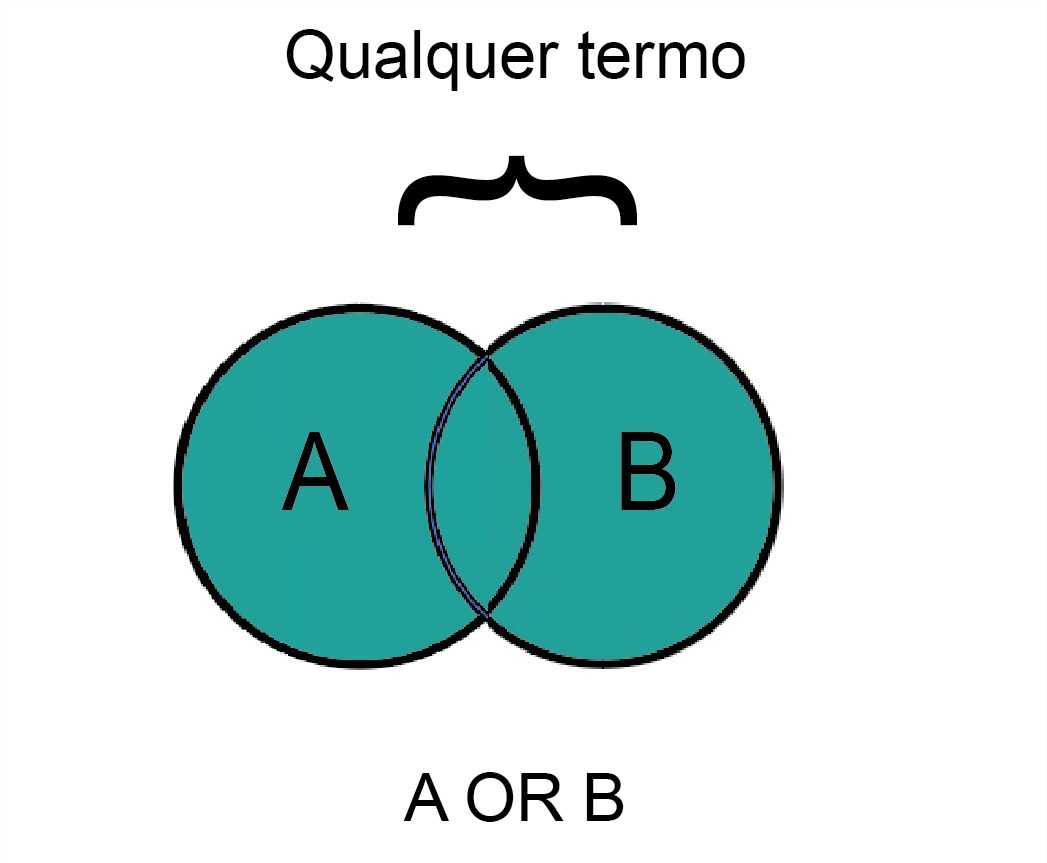
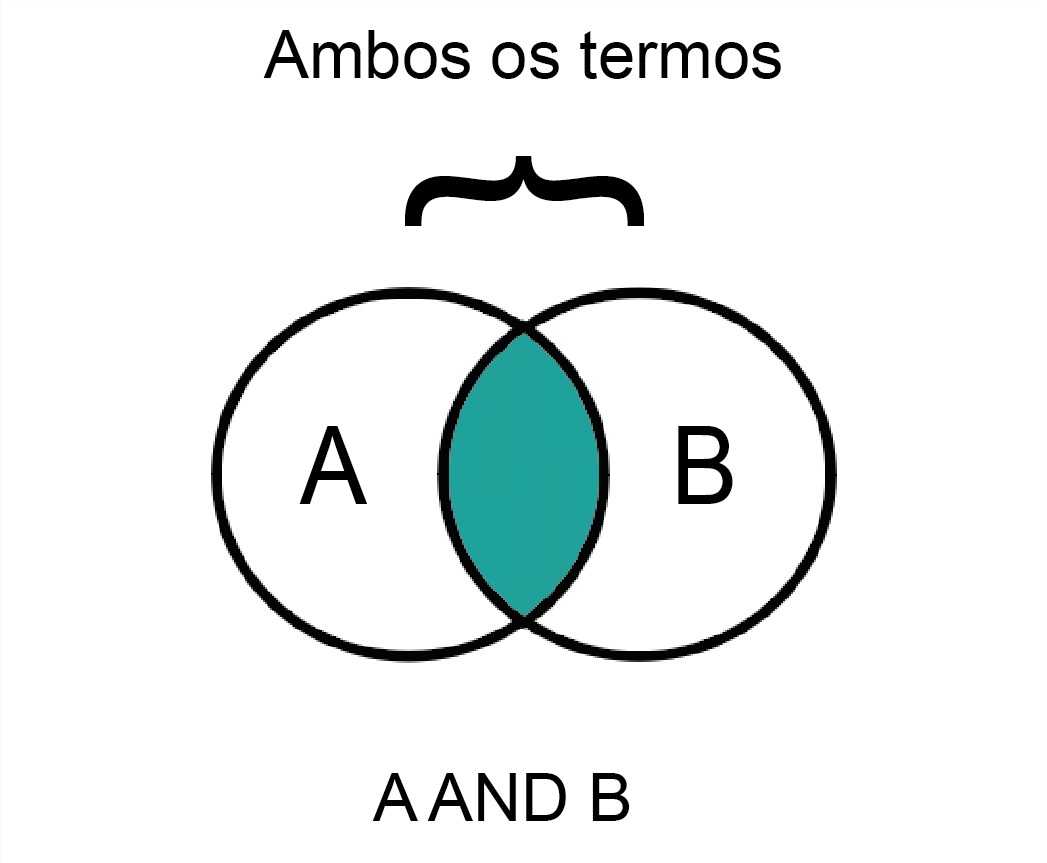
Precisão e Sensibilidade
Precisão é a capacidade da estratégia de busca de excluir artigos irrelevantes.
Sensibilidade é a capacidade da estratégia de busca de identificar todos os artigos relevantes.
O objetivo é maximizar a sensibilidade ao tentar maximizar a precisão.
Dicas e Truques
- Leve em consideração as diferenças de ortografia (por exemplo, inglês dos EUA versus inglês do Reino Unido)
- Considere o uso de outros campos PubMed, por exemplo, MeSH SubHeadings [SH] ou Pharmacological Action [PA]. Encontre mais informações aqui: Tags de pesquisa do PubMed
- Ao usar o operador NOT, leve em consideração qual literatura relevante você pode estar excluindo. - Considere símbolos de truncamento ou “curingas” para sua pesquisa (por exemplo, ischem* para ischemia e ischemic, etc). Verifique se todas as bases de dados bibliográficas permitem isso antes de adicionar à sua pesquisa.
6.3 Executando pesquisas e combinando resultados
Depois de ter composto os principais componentes da sua estratégia de busca, você pode executar pesquisas nas bases de dados de sua escolha.
1.Execute cadeias de busca em bases de dados especificadas.
O Polyglot Search Translator é uma ferramenta que o ajudará a traduzir a sintaxe de sua cadeia de busca em várias bases de dados. Para mais informações sobre o Polyglot Search Translator, clique aqui.
2.Combine os resultados em um software gerenciador de referências, como o EndNote ou Zotero
Para encontrar pdfs de textos integrais com mais facilidade, lembre-se de adicionar as informações de assinatura em bibliotecas nas configurações ou preferências do gerenciador de referências, por exemplo, informações de assinatura no EzProxy ou OpenURL.
A ordem de importação importa? SIM!
A ordem em que você importa suas referências para o Endnote ou outro gerenciador de referências é importante. Diferentes bases de dados bibliográficos têm qualidade ou completude diferente das referências nas quais você está interessado, e os gerenciadores de referência usam essas informações para deduplicar os resultados (o próximo passo).
A ordem recomendada é:
- Medline
- Embase
- Medline em processo (se incluído)
- Outras bases de dados do OvidSP (PsycInfo, EconLit etc)
- PubMed
- Cinahl Plus
- Outras bases de dados da Ebsco
- Bases de dados da Web of Science
- Scopus
- Bases de dados da ProQuest
- Bases de dados Cochrane
- Bases de dados CRD
- Quaisquer outras bases de dados
- Sites de ensaios clínicos
6.4 Deduplicação
Você pesquisou várias bases de dados diferentes e outras fontes. Provavelmente há duplicatas ou sobreposições. O tempo gasto na deduplicação de suas referências garantirá que você tenha números precisos (total de registros/incluídos/excluídos) para documentar e não perder tempo analisando duplicatas.
As ferramentas para ajudar a remover referências duplicadas incluem:
- O Endnote pode ser usado para localizar e remover registros duplicados. Veja este recurso.
- Ferramentas independentes, como a SR-Accelerator Tool e a ferramenta ASySD para revisões pré-clínicas.
6.5 Atualize sua pesquisa e ferramentas
O SyRF - Systematic Review Facility possui uma função integrada que pode recuperar automaticamente novos registros que atendam à sua cadeia de busca do PubMed. Para obter mais informações, consulte o Guia de Ajuda do SyRF aqui.
O Polyglot Search Translator é uma ferramenta que o ajudará a traduzir a sintaxe de sua cadeia de busca em várias bases de dados. Para mais informações sobre o Polyglot Search Translator, clique aqui.
6.6 Localizar e recuperar textos integrais
Depois de ter sua biblioteca de referências exclusivas, você pode encontrar e recuperar os textos integrais.
- Use seu gerenciador de referências. Guias para recuperação no Endnote e Zotero podem ser encontrados nos respectivos links.
OBS.: Lembre-se de adicionar suas informações de Login Institucional às configurações ou preferências do gerenciador de referências, por exemplo, do EzProxy ou OpenURL, para que você possa encontrar mais facilmente os textos integrais aos quais a biblioteca institucional tem acesso.
- Pesquisa Online: Pesquisa do Google, Google Scholar, ResearchGate, etc.
- Entre em contato com os autores correspondentes diretamente por e-mail ou Twitter.
- Último recurso: peça ao seu bibliotecário para ajudar com empréstimos entre bibliotecas. (OBS.: estes podem custar muito caro!)
OBS.: Tenha cuidado ao usar scripts personalizados ou outros programas para download em massa, pois isso pode resultar no bloqueio do seu endereço IP institucional!
Se a sua estratégia de busca tiver recuperado muitos resultados potencialmente relevantes, você pode considerar esperar para encontrar os textos integrais apenas depois de realizar a triagem de títulos e resumos (veja na próxima seção). Isso reduzirá bastante o número de registros de textos integrais que precisará encontrar e você não perderá tempo tentando encontrar artigos que não sejam relevantes para a sua pergunta de pesquisa.
7 Seleção de estudos
Depois de encontrar artigos que podem ser potencialmente relevantes para a sua pergunta de pesquisa, é necessário avaliar a relevância de cada artigo em relação a critérios predefinidos.
Se aplicável, você pode fazer isso em duas etapas:
- Triagem de Título ou Título e Resumo
- Triagem do texto integral
7.1 Critérios de Inclusão e Exclusão
Definir os critérios de inclusão e exclusão delimita a sua revisão. É importante que os critérios sejam pré-definidos,a priori, e aplicados de forma consistente em todos os estudos contemplados na revisão. Para garantir isso, é comum fazer triagem de citações em dupla, duas revisões independentes, com discussão ou um terceiro revisor independente para conciliar eventuais discordâncias.
Os critérios de inclusão referem-se a tudo que um estudo deve ter para ser incluído em sua revisão. Os critérios de exclusão referem-se a fatores que tornam um estudo inelegível para inclusão.
Normalmente, os critérios de inclusão e exclusão são definidos acerca de:
- Tipo de população (por exemplo, idade, sexo, modelo de doença)
- Tipo de intervenção (por exemplo, dosagem, tempo de intervenção, frequência)
- Tipo de Medição de Resultado (por exemplo, parâmetros relacionados ao método de avaliação ou aparelho)
Fatores adicionais que você pode querer levar em consideração:
- Restrições de idioma (quais idiomas sua equipe de revisão pode traduzir?)
- Restrições de data de publicação
- Tipo de publicação (por exemplo, resumos de conferências, revisão por pares)
Você pode considerar priorizar os critérios de inclusão e exclusão com base em quais critérios você provavelmente aplicará na fase de título e resumo e quais critérios você só poderá aplicar depois de ler o texto completo.
7.2 Aplique seus critérios
Um estudo foi incluído ou excluído em sua revisão? Um estudo é relevante, ou não relevante, para sua pergunta de pesquisa com base em seus critérios pré-definidos?
Para garantir que seus critérios de inclusão e exclusão sejam aplicados de maneira imparcial e uniforme, é uma boa escolha ter pelo menos 2 avaliadores independentes para aplicá-los. Se houver discrepâncias em suas decisões, você pode discuti-las até chegar a um consenso ou convidar um terceiro revisor independente para reconciliar quaisquer diferenças.
7.3 Ferramentas para triagem
Você pode fazer a triagem de títulos e resumos e de textos completos na SyRF - Systematic Review Facility, que é uma plataforma on-line de uso gratuito para auxiliar na condução da sua revisão sistemática pré-clínica.
A SyRF apresenta os artigos em ordem aleatória para os examinadores e, por padrão, exige um consenso entre múltiplos examinadores.
Outras plataformas de uso gratuito para realizar triagem de citações são Rayyan e SysRev.
8 Extração de dados
Extraia dados relevantes conforme definido em seu protocolo.
É uma prática recomendada extrair dados em duplicata, dois revisores independentes, para evitar erros.
8.1 Características do estudo
As características do estudo para extrair dos artigos incluídos incluem:
- Informações PICR (por exemplo, idade e sexo da população, espécie e linhagem do animal, dose e momento da intervenção, tipo e momento da avaliação do resultado)
- Informações sobre o design do estudo
- Informações sobre a qualidade do estudo veja na próxima seção)
- Informações adicionais (por exemplo, tempo entre a intervenção e a avaliação do resultado, qualquer informação sobre comorbidades)
8.2 Dados Quantitativos
A extração de dados quantitativos e numéricos de estudos incluídos é necessária para realizar a meta-análise para reunir os tamanhos de efeito
Seus resultados de interesse podem ser:
- Dicotômicos (por exemplo, mortalidade, presença de tumor)
- Contínuos (por exemplo, pressão arterial ou perda de peso)
- Dados de contagem (por exemplo, número de eventos)
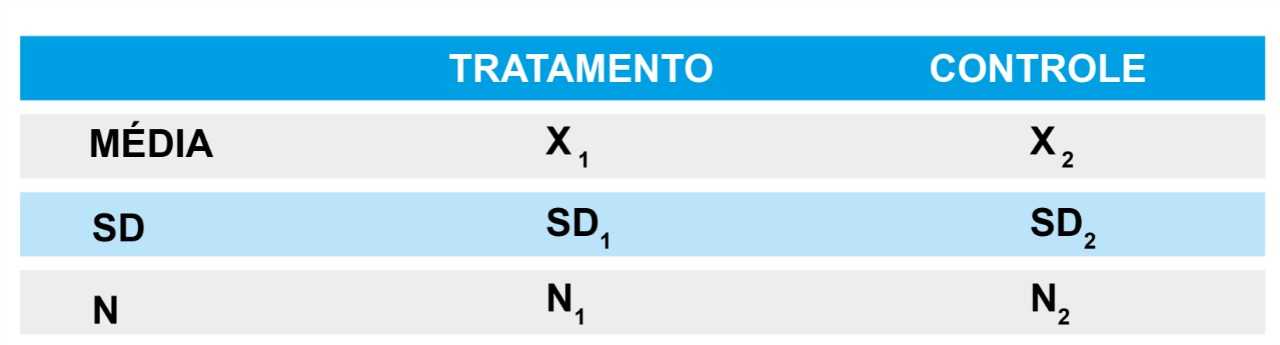
Os dados sobre seus resultados podem ser fornecidos em vários formatos, incluindo:
- Tabelas
- Texto
- Gráficos
Você pode precisar usar ferramentas como Adobe desktop ruler ou WebPlotDigitizer para extrair valores numéricos (por exemplo, médias e desvios padrão (SD) ou erro padrão da média (SEM) de gráficos). Alguns estudos podem relatar valores em uma escala diferente. Esteja ciente de que pode ser necessário convertê-los para uma escala comum a todos os estudos (por exemplo, conversão de escala logarítmica).
8.3 Software de extração de dados
À medida que essas informações são extraídas, você vai querer armazená-las no mesmo lugar para facilitar a síntese e análise posteriormente.
Recomendamos usar a SyRF - Systematic Review Facility para extrair e armazenar seus dados. É uma plataforma online gratuita onde você pode criar formulários de extração de dados personalizados para a sua revisão. Tipos flexíveis de perguntas e configurações de perguntas, bem como o formato on-line, permitem que você e sua equipe consigam extrair fácil e simultaneamente dados dos artigos incluídos. Para obter mais informações, consulte o site do SyRF e o Guia de ajuda do SyRF (inglês/português) para configurar seu projeto gratuito de revisão.
9. Avaliação de qualidade
Por que avaliar a qualidade do estudo?
A baixa qualidade metodológica pode afetar a validade interna e resultar em enviesamento nos resultados dos estudos primários. A validade interna refere-se a até que ponto os resultados do estudo refletem a verdadeira causa-efeito de uma intervenção. Diferentes tipos de viés podem influenciar a validade interna (por exemplo, vieses de seleção, desempenho, detecção e atrito).
Não é impacto. Não é novidade.
O viés em estudos primários pode levar a uma super ou subestimação do verdadeiro efeito da intervenção tanto em estudos primários quanto em revisões sistemáticas. É importante considerar as implicações da qualidade e validade do estudo para interpretar os resultados de sua revisão sistemática e muitas vezes é uma boa ideia incorporar uma seção de avaliação de qualidade em seu relatório final.
As características de qualidade do estudo que demonstraram impactar os resultados dos estudos pré-clínicos incluem se os animais foram randomizados para grupos de controle ou de tratamento e se os pesquisadores não tinham informações sobre o grupo de animais ao avaliar os resultados.
Leia mais sobre alocação e cegamento no site do NC3Rs Experimental Design Assistant
9.1 Relatórios
Use um checklist de verificação de qualidade para escrever os relatórios.
- Lista de Verificação do CAMARADES
- ARRIVE 2.0 Diretrizes para relatórios de pesquisas em animais
- Checklist de Relatórios da Nature. O checklist operacionalizado está disponível aqui.
9.2 Risco de viés
Para ajudá-lo a avaliar a qualidade do estudo, use uma ferramenta voltada à avaliação de qualidade ou risco de viés (Risk of Bias-RoB). Entre as ferramentas que foram desenvolvidas para avaliar o viés e a qualidade em estudos pré-clínicos, encontra-se a SYRCLE RoB.
9.3 Avaliação RoB para informar a análise
Um estudo que está em risco de ser tendencioso pode ter as conclusões impactadas por um viés. Os achados da avaliação de risco de enviesamento devem fazer parte das conclusões de sua revisão sistemática.
- Realize análise de sensibilidade (qualitativamente, ou quantitativamente usando meta-análise)
- Exclua estudos com alto risco de viés da síntese de evidências (isso deve ser feito com extrema cautela e deve ser pré-especificado em seu protocolo para evitar enviesamento)
- Chegue a uma conclusão geral para cada resultado sobre se o resultado sintetizado está em alto risco de viés
- Use a conclusão geral para informar a avaliação resumida da certeza da evidência usando, por exemplo, a abordagem GRADE
10 Meta-análise
O que é uma meta-análise?
Meta-análise é a combinação estatística de resultados de dois ou mais estudos separados
Por que realizar a Meta-análise?
- Para fornecer um teste com mais poder do que estudos separados
- Para fornecer uma melhoria na precisão estatística
- Para resumir descobertas numerosas e inconsistentes
- Para investigar a consistência do efeito em diferentes amostras
Que questões são abordadas?
- Qual é a direção do efeito?
- Qual o tamanho do efeito?
- O efeito é consistente entre todos os estudos? (heterogeneidade)
- Qual é a força da evidência para o efeito? (avaliação de qualidade)
(Referência: Cochrane Handbook)
Felizmente, software estatístico cuida da maior parte do 'trabalho pesado' quando se trata de calcular tamanhos de efeito, reuni-los e fazer gráficos de floresta (forest plots).
Para entender o básico e obter equações exatas, continue a leitura.
As equações mostradas abaixo são das seguintes referências, onde mais informações podem ser encontradas:
- “Meta-analysis of data from animal studies: a practical guide.” Journal of neuroscience methods - Vesterinen et al, 2014
- Introduction to Meta-Analysis - Borenstein et al., 2009
10.1 Etapa 1. Calculando tamanho do efeito
O primeiro passo é calcular o tamanho do efeito para cada resultado dentro de cada um dos estudos.
Seus resultados podem ser:
- Contínuos
- Dicotômicos
Contínuo
Para resultados contínuos, as medidas de tamanho de efeito comumente usadas incluem:
- Diferença Média
- Diferença de Médias Normalizadas
- Diferença de Médias Padronizadas
Diferença Média
Diferença média: A diferença média bruta pode ser usada quando os resultados são relatados em uma escala significativa e todos os estudos na análise usam a mesma escala. A meta-análise é realizada diretamente na diferença bruta nas médias.
Tamanho do Efeito da Diferença Média:
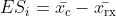
Erro padrão:
.png)
onde S combinado (pooled) é:
.png)
Diferença de Médias Normalizadas
Diferença de médias normalizadas: A diferença média normalizada (NMD) pode ser usada quando os resultados estão em uma escala de razão, onde a pontuação em um animal 'controle' ou 'placebo' é conhecida. O método mais comum para calcular o NMD é como uma proporção da média.
O cálculo do tamanho do efeito para a diferença média normalizada:
.png)
Onde
.png)
é a pontuação média para o animal não lesionado/normal/não tratado.
Os cálculos de desvio padrão são os seguintes:
.png)
e
.png)
O erro padrão do tamanho do efeito é:
.png)
Diferença de Médias Padronizadas
Diferença de médias padronizadas: (SMD), o D de Cohen e o G de Hedge. O SMD é usado quando a escala de medição difere entre os estudos e não é significativo combinar diferenças médias brutas. A diferença média em cada estudo é dividida pela divisão padrão do estudo para criar um índice comparável entre os estudos.
Tamanho do efeito (SMD) G de Hedge:
.png)
E o erro padrão do tamanho do efeito é:
.png)
Resultados dicotômicos
Para resultados dicotômicos, a medida de tamanho de efeito mais comumente usada para estudos em animais é a razão de chances.
Razão de Chances
Razão de chances:: para dados de eventos. A razão entre o número de eventos e o número de não eventos. Ela representa as chances de um resultado ocorrer dada uma determinada exposição, em comparação com as chances de o resultado ocorrer sem essa exposição.
Tamanho do Efeito da Razão de chances:
.png)
com o erro padrão:
.png)
Você pode encontrar a Razão de Risco (ou Risco Relativo), que é o risco de um evento em um grupo (por exemplo, grupo exposto) versus o risco do evento em outro grupo (por exemplo, grupo não exposto), ou a Razão de Perigo; no entanto, esses dados raramente são vistos em experimentos primários com animais. Para obter mais informações sobre a Razão de Risco em revisões sistemáticas clínicas, consulte o Cochrane Handbook.
Mediana
Sobrevivência mediana ou dado de tempo para evento. O efeito é calculado dividindo a sobrevivência mediana no grupo de tratamento pela mediana no grupo controle, e o logaritmo é obtido.
.png)
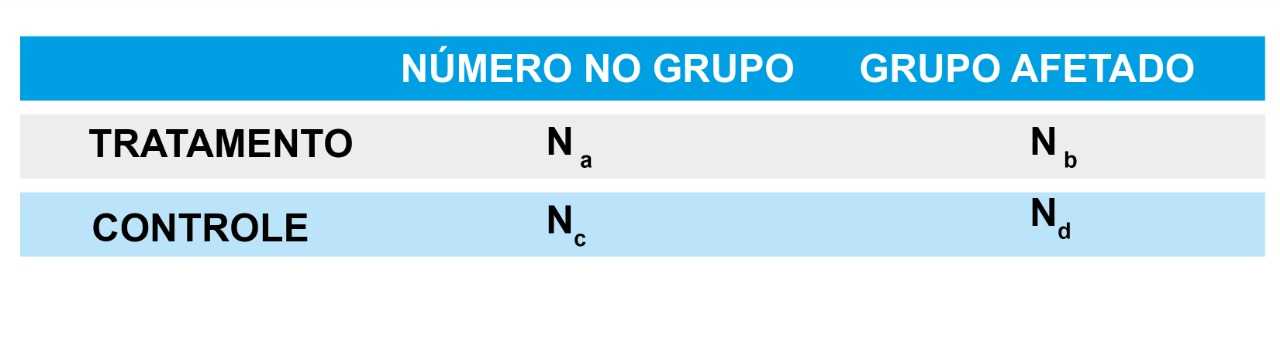
Número real dos controles
Um único experimento pode conter várias comparações. Se o coorte de controle estiver atendendo a mais de um grupo de tratamento, corrigimos o número de animais relatados no coorte de controle pelo número de grupos de tratamento.
- Número real dos controles
![Formula]()
- Número real para cada comparação
![Formula]()
- Convertendo SEM para SD
![Formula]()
- e
![Formula]()
10.2 Etapa 2. Combinar tamanhos do efeito
O próximo passo é combinar os tamanhos do efeito para cada comparação em um modelo de meta-análise.
Antes de agrupar os tamanhos do efeito, você pode querer levar em consideração:
Pesos dos Tamanhos do Efeito: na meta-análise, é comum atribuir pesos diferentes a cada estudo para refletir as contribuições relativas de estudos individuais para o tamanho total do efeito. Na meta-análise de estudos animais, pesamos os estudos de acordo com a precisão. Estudos mais precisos recebem maior peso no cálculo do tamanho do efeito. Recomendamos usar o método de variância inversa, onde os tamanhos de efeito individuais são multiplicados pelo inverso de seu erro padrão ao quadrado:
.png)
Onde:
.png)
é o erro padrão ao quadrado do tamanho do efeito calculado.
Isso fornece o peso do tamanho do efeito de:
.png)
Efeitos de aninhamento: quando vários resultados são relatados e é apropriado combiná-los em uma única estatística, podemos “aninhar” os resultados. Para fazer isso, pegamos cada resultado, calculamos o peso multiplicando pelo inverso da variância desse resultado, somamos esses valores para todos os resultados e dividimos pela soma dos pesos.
.png)
Onde
.png)
é a medida do peso (por exemplo, variância inversa).
.png)
é o peso do tamanho do efeito e k denota o número total de estudos incluídos na meta-análise.
O erro padrão é calculado:
.png)
Existem dois modelos comumente usados para agrupar tamanhos de efeito:
- Modelo de Efeito Fixo
- Modelo de Efeitos Aleatórios
A seleção de qual modelo usar deve ser declarada em seu protocolo a priori. A decisão é baseada na natureza dos estudos que provavelmente serão incluídos em sua revisão. O modelo de efeitos aleatórios é mais comumente usado em estudos pré-clínicos, pois geralmente são sintetizados dados de estudos realizados em diferentes laboratórios e é esperado que exista heterogeneidade. Muitas vezes sintetizamos dados de experimentos onde a espécie, idade ou sexo dos animais são diferentes, a intervenção pode ser dada em doses variadas ou em momentos diferentes em relação ao resultado. Assumimos que essas variáveis de design do estudo têm um impacto sobre os efeitos que vemos nos estudos.
Raramente, ao fazer uma revisão sistemática de dados de um laboratório específico, se todos os estudos em sua meta-análise foram realizados usando o mesmo modelo de indução, paradigmas e intervenções, você pode considerar um modelo de efeito fixo. (Borenstein et al., 2009)
Modelo de Efeitos Fixos
Sob o modelo de efeito fixo, assumimos que existe um tamanho de efeito real que é compartilhado por todos os estudos incluídos. Segue-se que o efeito combinado (estimativa global) é nossa estimativa desse tamanho de efeito comum.
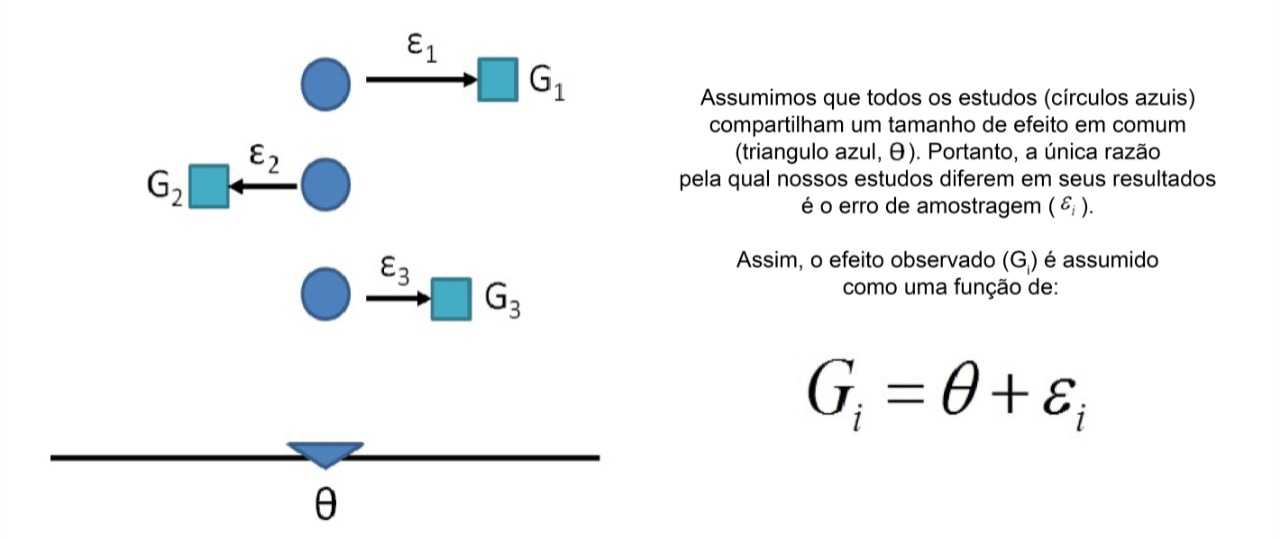
Modelo de Efeitos Aleatórios
- Sob o modelo de efeitos aleatórios, permitimos que o efeito real possa variar de estudo para estudo. Por exemplo, o tamanho do efeito pode ser um pouco maior se os pacientes forem mais velhos; em ratos vs. camundongos; se o estudo usou uma variante um pouco mais intensiva ou mais longa da intervenção, etc.
- Os estudos incluídos na meta-análise são considerados uma amostra aleatória da distribuição relevante de efeitos, e o efeito combinado estima o efeito médio nessa distribuição.
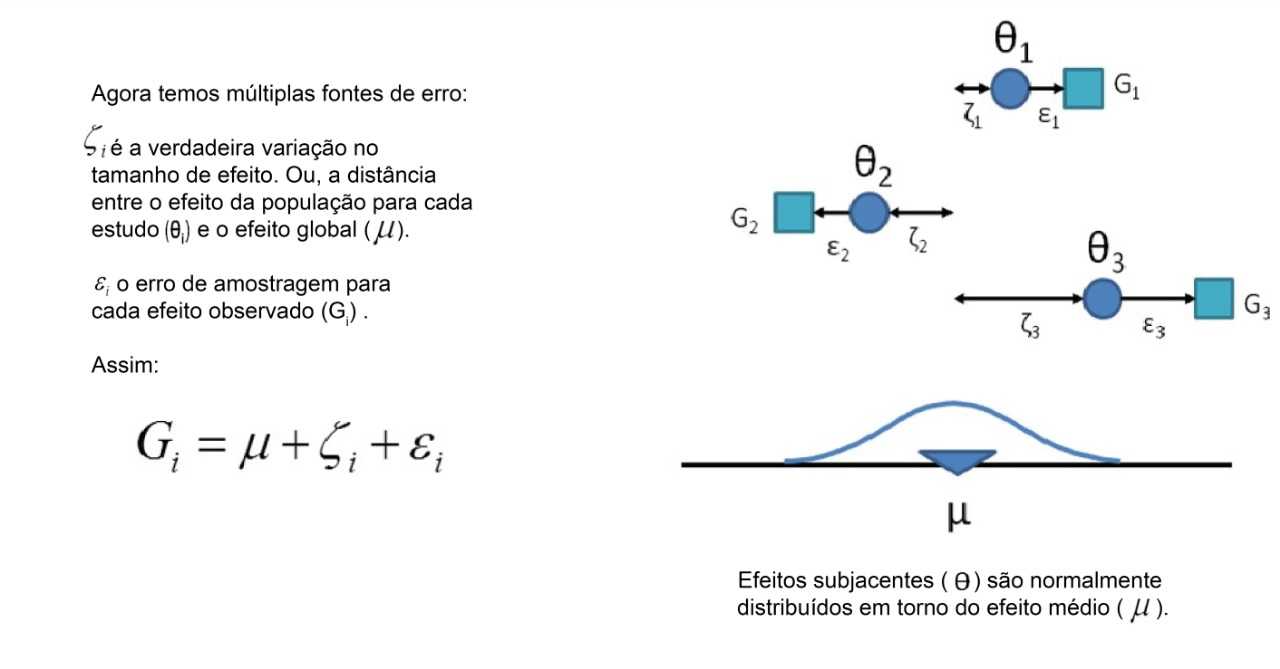
10.3 Etapa 3. Investigar a Heterogeneidade
A terceira etapa é investigar possíveis fontes de heterogeneidade (pré-especificadas em seu protocolo). A heterogeneidade é a variabilidade entre grupos de estudos causada por diferenças em:
- amostras de estudo (por exemplo, espécie, sexo)
- intervenções de resultados (por exemplo, dose, tipo de medição de resultado)
- metodologia (por exemplo, design, qualidade)
Qui-quadrado χ2 (ou Qui2) avalia se as diferenças observadas nos resultados são compatíveis apenas com o acaso. I2 descreve a porcentagem de variabilidade nas estimativas de efeito que se deve à heterogeneidade e não ao erro de amostragem ou ao acaso.
Você pode investigar a heterogeneidade usando:
- Análise de subgrupo
- Modelo de meta-regressão
10.4 Etapa 4. Documentando Enviesamento
O viés de publicação ocorre quando os resultados de estudos publicados e não publicados diferem sistematicamente. Infelizmente, estudos neutros e negativos demoram mais para serem publicados, permanecem sem serem publicados, têm menor probabilidade de serem identificados em revisão sistemática, e isso pode levar a uma superestimação da eficácia na meta-análise.
Há também outros vieses que podem afetar sua revisão sistemática, incluindo relato de resultados e análises selecionadas.
Podemos testar um possível viés de publicação em nossos dados colocando-os em um gráfico de funil. As linhas tracejadas externas indicam a região triangular na qual se espera que 95% dos estudos se encontrem, na ausência de vieses e heterogeneidade. A linha vertical sólida refere-se à linha sem efeito. Imagem adaptada de Sterne et al., 2011
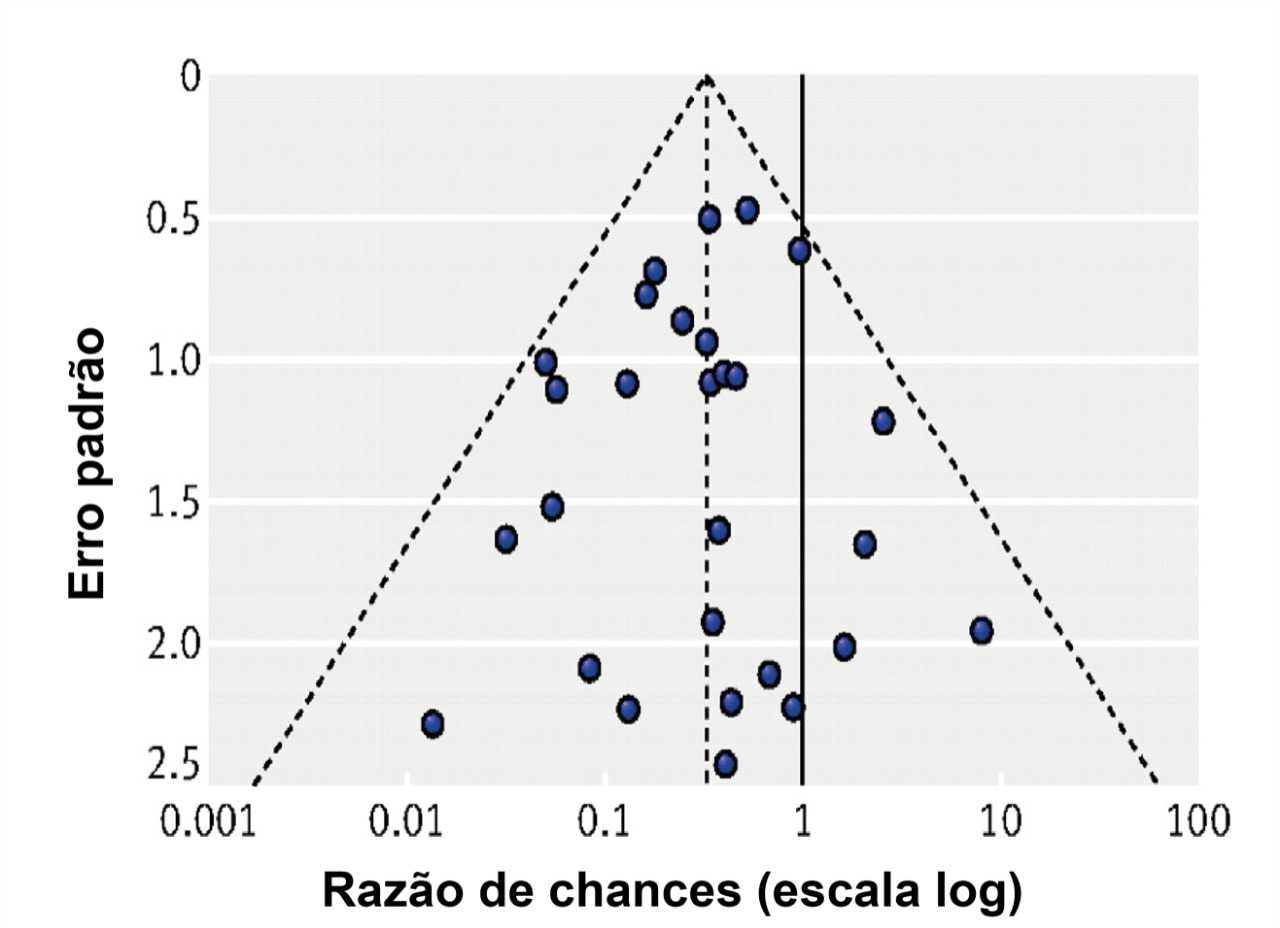
Se você observar assimetria em seu gráfico de funil, pode haver várias razões:
- Documentações Enviesadas
- Viés de Publicação
- Relatório seletivo dos resultados
- Relatório seletivo das análises
- Má qualidade metodológica (levando a efeitos inflados em estudos menores)
- Mau desenvolvimento metodológico
- Análise inadequada
- Fraude
- Heterogeneidade real: o tamanho do efeito difere de acordo com o tamanho do estudo devido, por exemplo, às diferenças na intensidade das intervenções ou no risco subjacente entre estudos com tamanhos diferentes.
- Artefatos: a variação amostral pode levar a uma associação entre o efeito da intervenção e seu erro padrão.
- Acaso: a assimetria pode ocorrer por acaso - motivando o uso de testes estatísticos de assimetria.
10.5 Etapa 5. Interpretando os Resultados
O gráfico de floresta (forest plot) ou timber plot é a principal representação gráfica de uma meta-análise.
Ler e entender esses gráficos permitirá que você entenda os resultados de uma meta-análise. Meta-análises de estudos em animais tendem a incluir muitos estudos com amostras pequenas. Portanto, é comum ver meta-análises pré-clínicas representadas graficamente com um timber plot, uma pequena variação do gráfico de floresta.
Aqui está um exemplo de um timber plot. Nesta meta-análise a pergunta de pesquisa foi: Qual é o efeito dos antidepressivos comparados com o veículo ou com o não tratamento no volume do infarto em modelos animais de acidente vascular cerebral isquêmico? Adaptado de McCann et al., 2014
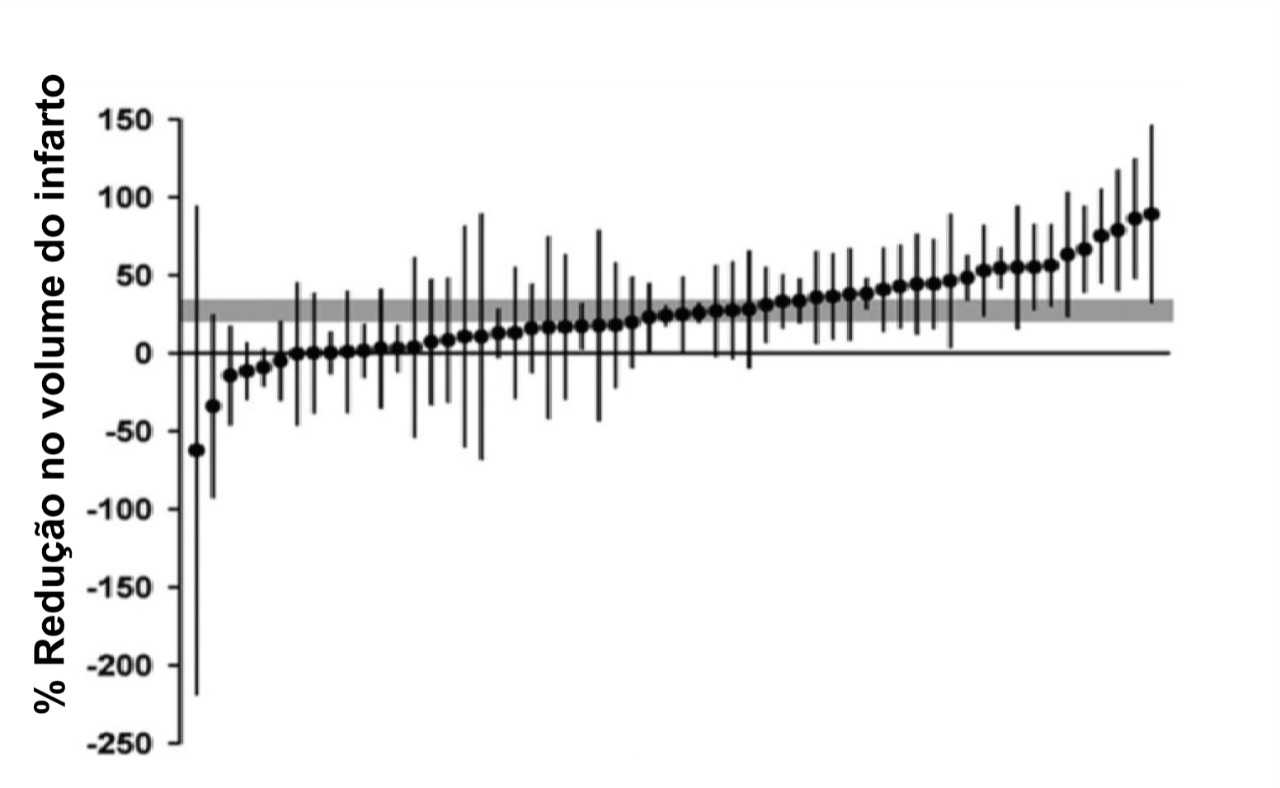
Resultado: uma meta-análise é conduzida com base em um único resultado de interesse de cada vez. O resultado de interesse nesta meta-análise é a redução do volume do infarto, conforme exibido no rótulo do eixo y.
Efeitos individuais do estudo: nesta meta-análise foram incluídos 58 experimentos. Cada ponto preto representa o tamanho do efeito relatado em um único experimento, a diferença no resultado entre a média e o grupo de controle. Cada ponto preto tem linhas pretas finas acima e abaixo do tamanho do efeito, que representam as margens de erros associadas ao tamanho do efeito relatado. Os tamanhos de efeitos individuais de estudo são exibidos em ordem do menor para o maior para destacar a variação ou heterogeneidade na literatura.
Efeito agrupado: aqui, a barra cinza atrás dos pontos pretos representa o tamanho do efeito combinado ou agrupado em todos os experimentos incluídos e seus intervalos de confiança (IC). Neste exemplo, o tamanho do efeito é 27,3% (IC 95%, 20,7%–33,8%).
Gráfico de floresta para meta-análise clínica: Um guia passo a passo para interpretar um gráfico de floresta a partir de uma meta-análise clínica típica está disponível aqui.
11 Ferramentas para Revisão Sistemática
É altamente recomendável usar softwares e ferramentas para ajudá-lo ao longo do caminho. Mencionamos muitas ferramentas ao longo deste Wiki, aqui está uma lista de todas elas:
SyRF - Systematic Review Facility é uma plataforma online de uso gratuito para auxiliar na sua revisão sistemática pré-clínica. Seus recursos e ferramentas auxiliares incluem:
- Atualização automática da sua busca no PubMed
- Deduplicação de buscas sistemáticas no AsysD App
- Triagem (título e resumo, bem como texto completo)
- Anotação e extração de dados
- Meta-análise de dados do SyRF clique aqui
As ferramentas adicionais incluem:
- Triagem de citações: Rayyan e SysRev.
- Extração de dados de gráficos: Adobe desktop ruler ou WebPlotDigitizer
- Tradução de pesquisa em bases de dados: Polyglot Search Translator
Machine Learning - se você estiver fazendo uma grande revisão sistemática, considere aprender ML. Entre em contato conosco para mais informações.
12 Publicação
Você realizou sua revisão sistemática e, potencialmente, também conduziu uma meta-análise, agora é hora de contar à comunidade o que você encontrou e garantir que as descobertas da revisão cheguem ao público.
Tenha cuidado ao interpretar os resultados; reconheça fontes de enviesamento; leve em consideração a heterogeneidade, generalização e relevância.
Pode ser útil usar uma abordagem GRADE para avaliar a certeza da evidência de estudos pré-clínicos em animais, no contexto de intervenções terapêuticas.
Apresente sua revisão sistemática de forma que permita a reprodutibilidade dos resultados e atualização futura.
12.1 Produzindo um bom relatório
Recomendamos seguir as Diretrizes de Itens de Documentação Preferenciais para Revisões Sistemáticas e Meta-análises (Preferred Reporting Items for Systematic Reviews and Meta-analyses - PRISMA).
Um checklist de verificação pode ser encontrado aqui
Recomendamos usar o fluxograma PRISMA para visualizar os estudos em seu processo de revisão sistemática. O modelo de fluxograma PRISMA pode ser encontrado aqui.

13 Recursos e links
Protocolo SYRCLE - Template & Paper
Hooijmans et al., 2018. Abordagem pré-clínica GRADE
14. Sobre
Criamos esta página Wiki para fornecer informações e documentos, links e ferramentas úteis para guiá-lo através de sua revisão sistemática pré-clínica. Esses recursos foram reunidos usando muitas fontes CC-BY-4.0, incluindo: SyRF e Cochrane Interactive Learning. Agradecemos a essas organizações e equipes por disponibilizarem seus recursos, que você também deve visitar!
Este recurso foi atualizado pela última vez em: 15 dezembro, 2021
14.1 Como citar a ferramenta?
CAMARADES Berlin. WIKI de Revisão Sistemática Pré-clínica e Meta-Análise. Tradução por CAMARADES Brasil. Outubro, 2021. Disponível em https://camaradesbrasil.bio.br/. Acessado em 11 de ago. de 2023.
14.2 Equipe do conteúdo original
- Sarah McCann, PhD
- Torsten Rackoll, PhD
- Alexandra Bannach-Brown, PhD
- Florenz Cruz
14.3 Equipe de tradução
- Tamires Martins, Ms
- Juliana Aparecida Bolzan, Ms
- Cilene Lino de Oliveira, PhD
Se você tiver dúvidas sobre os recursos ou gostaria de fazer uma pergunta sobre sua revisão especificamente, entre em contato: envie-nos um e-mail aqui
O recurso é apoiado por Charité 3Rs. Para obter mais informações sobre os 3Rs na Charité – Universitätsmedizin Berlin, visite o Charité 3Rs Toolbox.

A tradução do conteúdo deste recurso do inglês para o português foi apoiada pela Fundação Alexander von Humboldt. Para mais informações visito o site.

CAMARADES Berlin está localizado no QUEST Center, Berlin Institute for Health
CAMARADES BR está localizado no Laboratório de Neurobiologia do Comportamento (LabNeC-CFS-CCB) da Universidade Federal de Santa Catarina (UFSC).
14.3 Demais apoiadores
14.4 Contato
Se você tiver dúvidas sobre os recursos, quiser fazer uma pergunta específica ou contribuir para o texto, entre em contato conosco aqui
.png)
.png)
.png)
.png)




