Um guia para Farmacologistas
Boas vindas!
Olá, farmacologistas!
Bem-vindos ao wiki SysPhar Revisões Sistemáticas em Farmacologia
No guia SysPhar você encontra informações, links, artigos, recursos e ferramentas úteis para conduzir suas revisões sistemáticas e meta-análises em Farmacologia.
Navegue pelas seções para descobrir como planejar, conduzir e concluir uma revisão sistemática, uma meta-análise ou uma revisão sistemática viva.
Use a barra de índice no lado esquerdo da tela para navegar pelas etapas do nosso guia.
1 Revisão Sistemática e Meta-análise
1.1 O que é Revisão Sistemática?
Revisões sistemáticas* são revisões da literatura realizadas com os objetivos de identificar, obter, filtrar, avaliar e sintetizar estudos científicos para responder a uma questão de pesquisa. Usam métodos transparentes, baseados em decisões tecnicamente fundamentadas e imparciais; portanto, são reproduzíveis.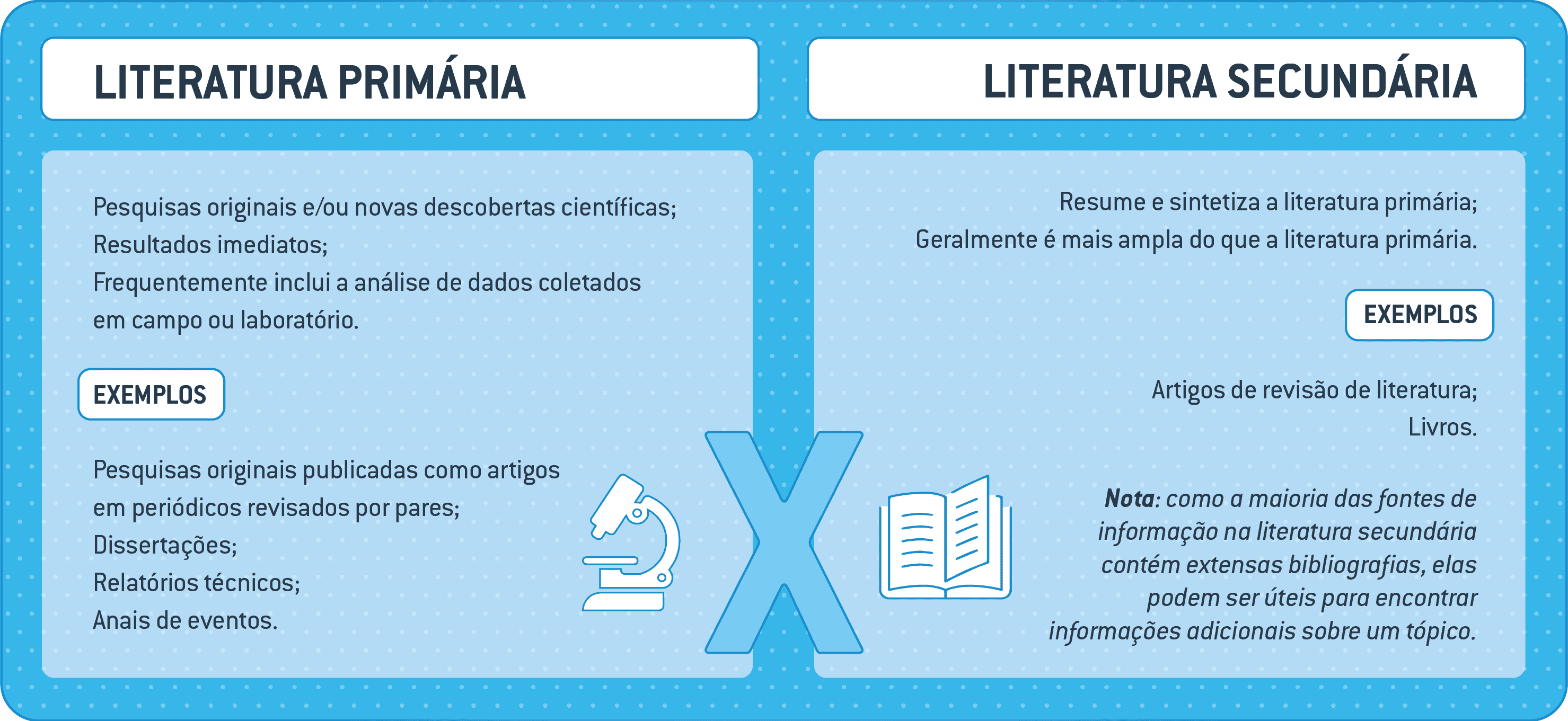
Referências sugeridas: Cook, Mulrow e Haynes (1997);Gopalakrishnan e Ganeshkumar (2013); Delgado-Rodríguez e Sillero-Arenas (2018).
*Nota: uma revisão sistemática pode ou não ser seguida de uma meta-análise.
1.2 O que é meta-análise?
Meta-análise* é um método estatístico utilizado para combinar os resultados quantitativos de dois ou mais estudos primários independentes, sintetizando-os em um resultado único.
Referências sugeridas: Haidich (2010); Vesterinen et al. (2014); Møller e Myles (2016); Wormald e Evans (2018).
1.3 O que é revisão sistemática e meta-análise viva?
As revisões sistemáticas e meta-análises podem rapidamente se tornar obsoletas, às vezes antes mesmo de serem finalizadas.
As abordagens de atualização que incorporam novas evidências relevantes à medida que estas se tornam disponíveis são chamadas de “revisões sistemáticas e meta-análises vivas”, ou living systematic reviews (LSR), em inglês.
Referências sugeridas: Elliott et al. (2014); Garner et al. (2016); Elliott et al. (2017); Simmonds et al. (2022).
1.4 Revisões sistemáticas e meta-análises em farmacologia
No contexto da Farmacologia, estudos únicos nem sempre são suficientes para fornecer informações confiáveis a favor ou contra o uso de um fármaco em um experimento, projeto ou no desenvolvimento de um medicamento.
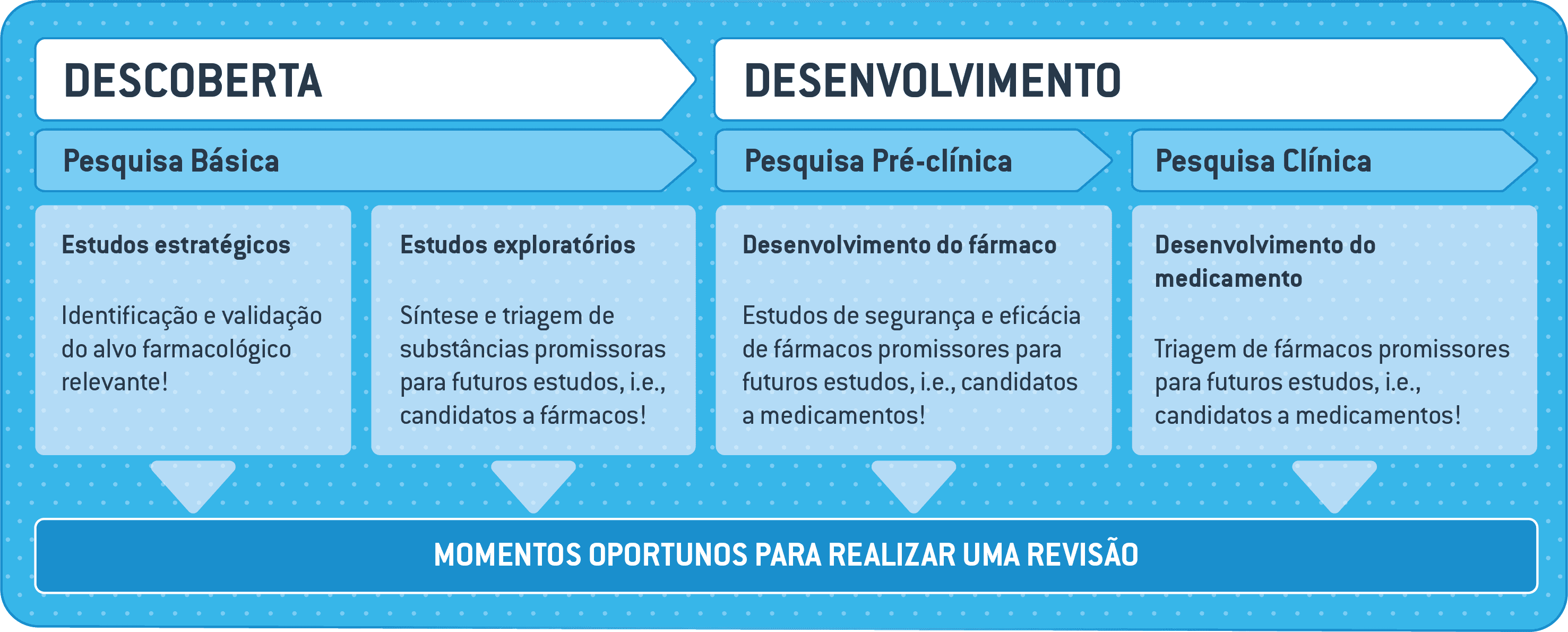
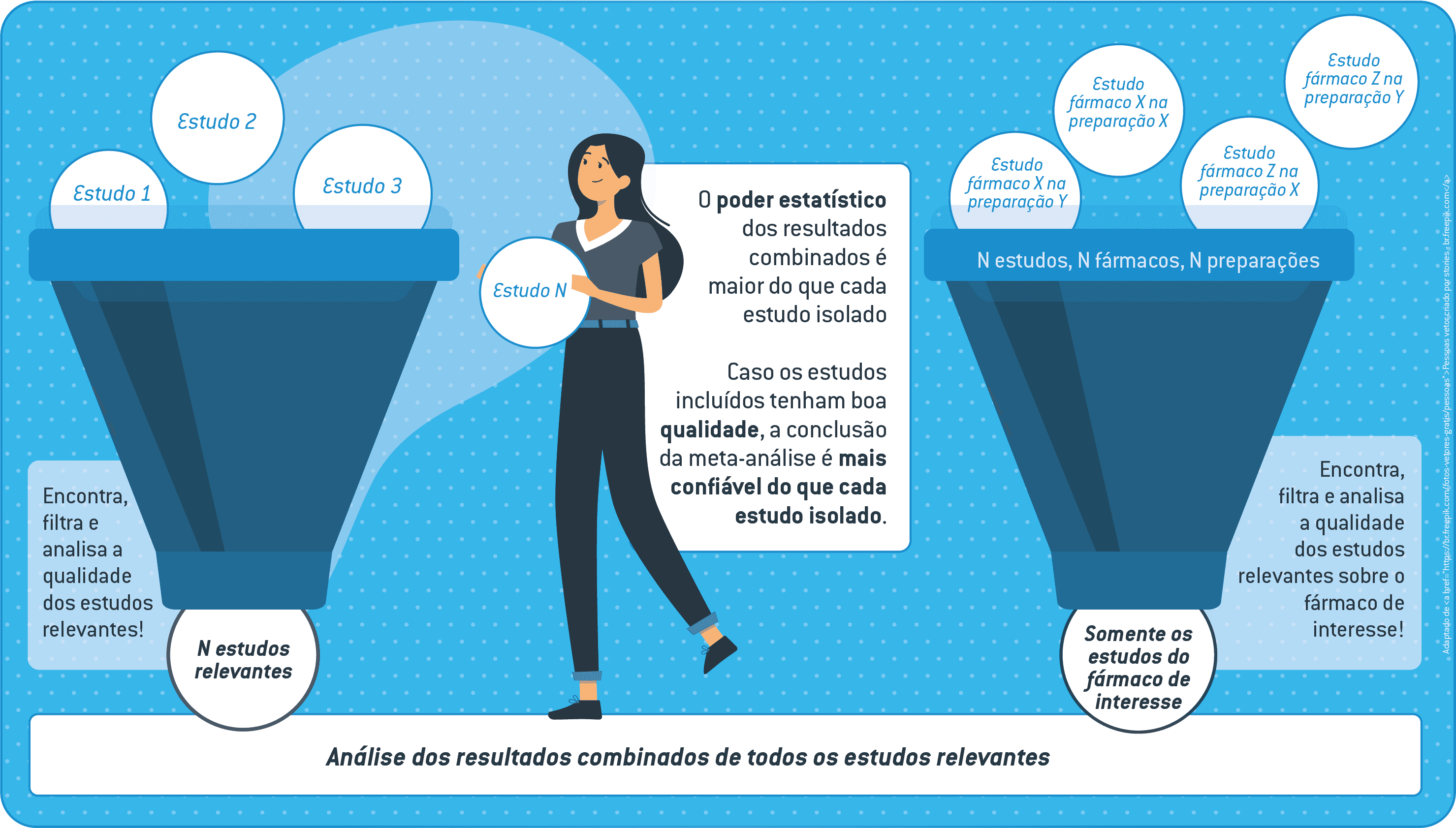
Referências sugeridas: Lino de Oliveira et al. (2020); Hesen et al. (2017); Al-Waeli et al. (2021). Veja revisões sistemáticas em farmacologia na aba “Portfólio & Iniciativas”
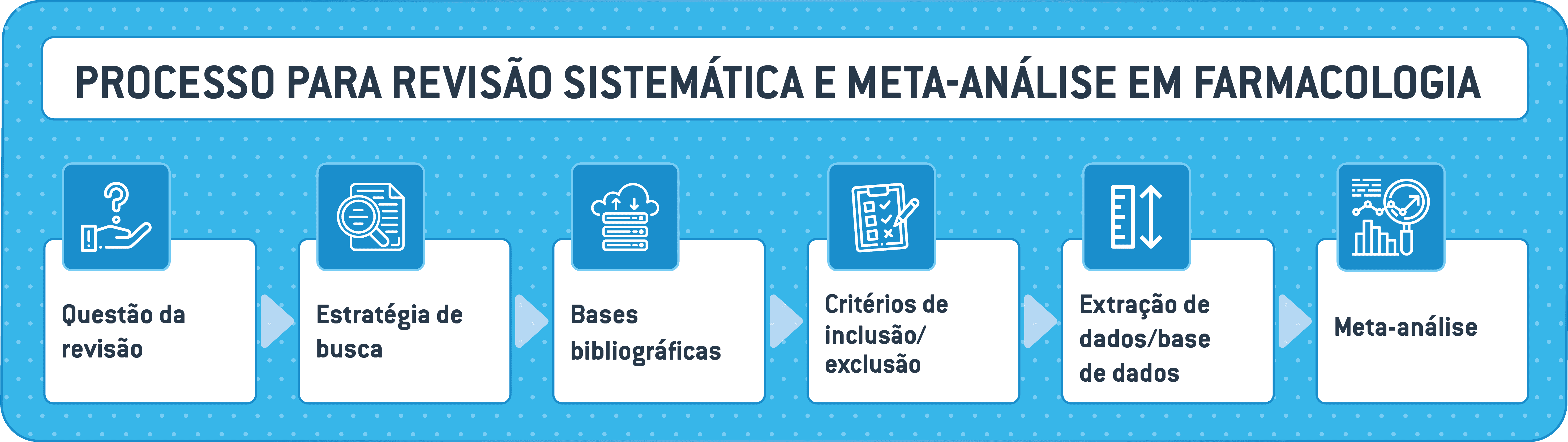
2 Plano geral das Revisões Sistemáticas e Meta-análises
2.1 Planejamento, implementação, publicação e manutenção
Aqui no SysPhar, o plano geral das revisões sistemáticas e meta-análises – cujo fluxograma é apresentado na Figura 5 – é dividido em fases sequencialmente organizadas: inicia com a fase 0, antes de começar o processo; passa pelas fases de 1 a 5, nas quais a pergunta da pesquisa é formulada, o protocolo é elaborado, registrado e implementado, e os resultados são publicados; e termina na fase 6, em que se mantêm a revisão sistemática e meta-análise vivas. É muito recomendável que estas etapas sejam realizadas nesta ordem, para que as decisões analíticas e metodológicas sejam todas tomadas antes que as ações analíticas e metodológicas sejam realizadas.
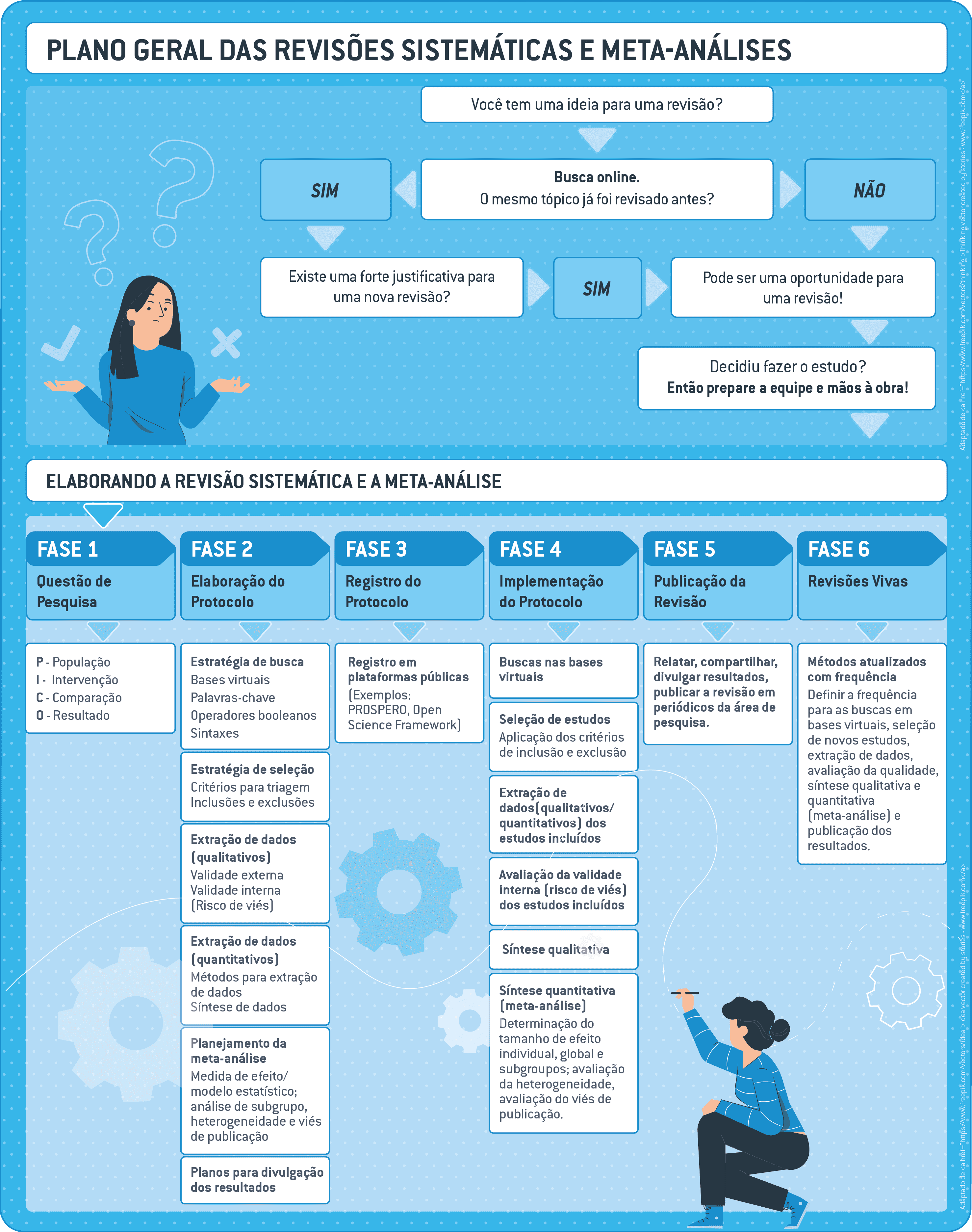
*Nota: nem toda revisão sistemática precisa ser seguida de uma meta-análise e nem toda revisão sistemática e meta-análise precisa se tornar viva. Cada farmacologista deve decidir de acordo com as demandas do tema e objetivos de sua pesquisa.
3 Fase 0: Antes de começar
3.1 Relevância do estudo
Revisões sistemáticas e meta-análises são trabalhosas, custam tempo e recursos humanos. Por isso, sugerimos fortemente que ANTES DE COMEÇAR, o farmacologista interessado em usar estas abordagens faça uma análise prévia do contexto de uma revisão sistemática e meta-análise em farmacologia no tema de seu interesse, respondendo às seguintes perguntas:

Se você respondeu “sim” às perguntas de 1 a 5 e “não” à pergunta 6, é possível que sua revisão tenha relevância científica e tecnológica e seja original. Portanto, prepare sua equipe!
Caso você tenha respondido “sim” também à pergunta 6, ou seja, se a revisão de seu interesse já estiver em andamento, considere entrar em contato com a equipe dessa revisão para uma possível colaboração.
*Nota: para verificar se o tema foi previamente revisado, faça uma busca em bases bibliográficas relevantes para a Farmacologia, como a Medline via Pubmed, Scopus, Web of Science e Embase. Também considere usar plataformas de pré-impressão, por exemplo a bioRxiv, medRxiv e OSF, ou usar depósitos de revisões sistemáticas em andamento, como a PROSPERO.
3.2 Preparando a equipe para começar
Para o planejamento, implementação, publicação e manutenção de uma revisão sistemática e uma meta-análise em Farmacologia, a equipe ideal seria formada por:
- farmacologistas: responsáveis pela seleção do tema, elaboração da pergunta da revisão relevante em Farmacologia e elaboração do protocolo (ex., ajudando a identificar os aspectos relevantes para o escopo da busca, para a seleção dos estudos, e para a análise dos dados)
- bibliotecários(as) ou especialistas em revisões sistemáticas da literatura: responsáveis pela elaboração do protocolo (ex., ajudando a criar as estratégias de busca na literatura), recomendação de softwares, ferramentas e abordagens de busca e seleção de literatura relevante para a pergunta da revisão.
- estatísticos(as) ou especialistas em meta-análise: responsáveis pela elaboração do protocolo (ex., ajudando a selecionar os tipos de cálculos de tamanho de efeito e modelos estatísticos de acordo com os desfechos de interesse) e recomendação de softwares, ferramentas e abordagens para fazer a análise dos dados.
- revisores(as): responsáveis pela realização das etapas menos especializadas do processo (ex., seleção de estudos aplicando critérios pré-estabelecidos, extração de dados de acordo com o protocolo e tabulação dos dados extraídos dos estudos). Mesmo revisores principiantes podem contribuir nas etapas de implementação do protocolo de revisão, sob a supervisão de membros mais experientes da equipe. Estes revisores podem ser recrutados durante a realização dos trabalhos.
Pode ser útil criar papéis específicos para cada membro da equipe. Cada papel pode ser desempenhado por mais de uma pessoa e cada pessoa pode desempenhar mais de um papel simultaneamente.
- Líder: responsável pelo gerenciamento das atividades da equipe e dos documentos da revisão*.
- Revisor independente 1: responsável por aplicar critérios de elegibilidade dos estudos, extrair e tabular os dados dos estudos incluídos na revisão de forma independente do revisor 2.
- Revisor independente 2: responsável por aplicar critérios de elegibilidade dos estudos, extrair e tabular os dados dos estudos incluídos na revisão de forma independente do revisor 1.
- Revisor 3 (conciliador): responsável por conciliar as discrepâncias entre os revisores independentes 1 e 2.

*Nota: no início do processo de revisão, é importante registrar e armazenar todos os documentos relacionados à revisão em um local de compartilhamento (exemplo:OSF,Google Drive,OneDrive), para que toda a equipe tenha acesso.
4 Fase 1: elaborando a pergunta da revisão
A definição da questão ou pergunta da pesquisa guiará todas as decisões nas fases subsequentes de uma revisão sistemática e meta-análise. Frequentemente, as perguntas de pesquisa em Farmacologia assumem estruturas semelhantes a estas:
- O fármaco X é eficaz na cura ou melhora de uma condição Y em um tipo específico de experimento ou teste?”;
- “Existe uma relação dose-resposta entre o fármaco X e a resposta Y?”;
- “Uma população (de ratos, camundongos, humanos, preparações in vitro, etc.) é suscetível aos efeitos do fármaco X?”;
- Uma subpopulação da amostra (espécie, linhagem, sexo etc.) é mais ou menos suscetível aos efeitos do fármaco X?”.
4.1 Ferramenta PICO
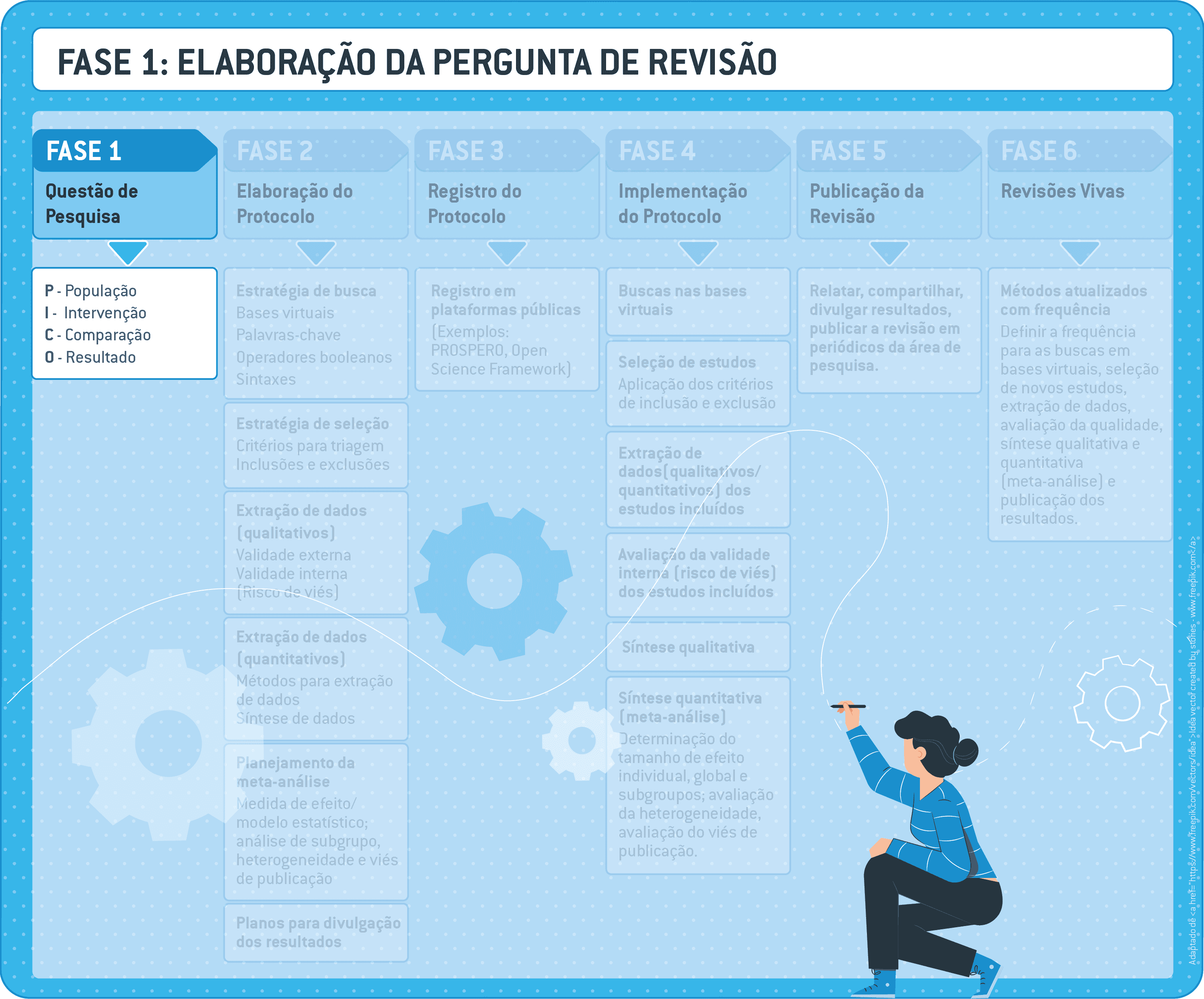
A ferramenta PICO (P – Paciente ou população ou problema; I – Intervenção; C – Comparação ou Controle; O – Outcome ou Desfecho), desenvolvida para revisar ensaios clínicos controlados e randomizados, é também adequada para revisões de estudos não-clínicos em Farmacologia.
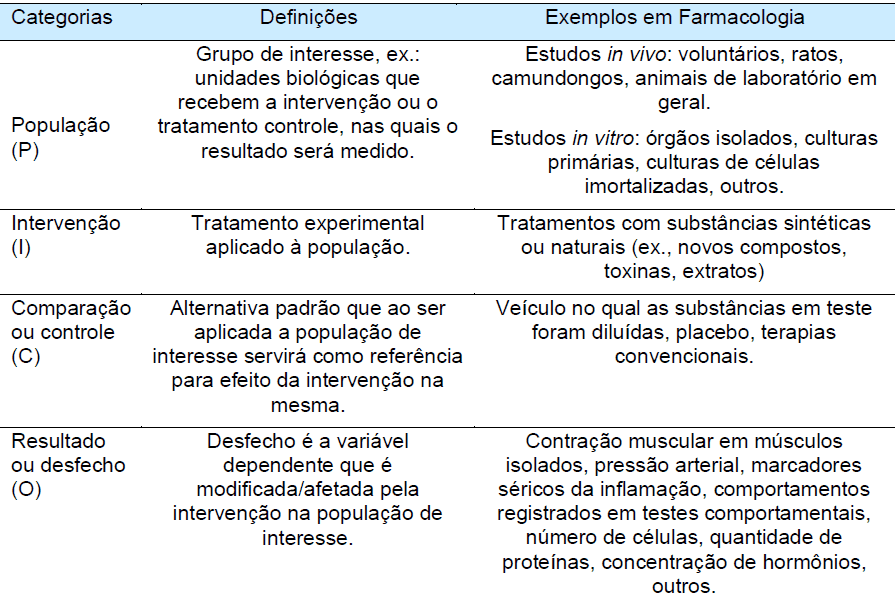
Fonte: adaptado de Bolzan e Lino de Oliveira (2022).
Referências sugeridas: Schardt et al., (2007); Eriksen e Frandsen (2018).
4.2 Outras ferramentas mnemônicas
Outras ferramentas mnemônicas podem ser úteis para fazer perguntas em alguns tipos específicos de pesquisa in vitro, in vivo, ex vivo em Farmacologia.
São exemplos de alternativas à ferramenta PICO: o PICOC (PICO mais Contexto); PICOT (PICO mais Tempo); SPICE (S – Setting ou contexto experimental; P – População; I – Intervenção; C – Comparação; E – Evaluation ou Avaliação); e a SPIDER (S – Sample ou Amostra de interesse; P – Phenomenon ou Fenômeno de Interesse; D – Desenho Experimental; E – Evaluation ou Avaliação; R – Research type ou Tipo de pesquisa).
Referências sugeridas: Cooke, Smith e Booth (2012); Wohlin et al., (2012).
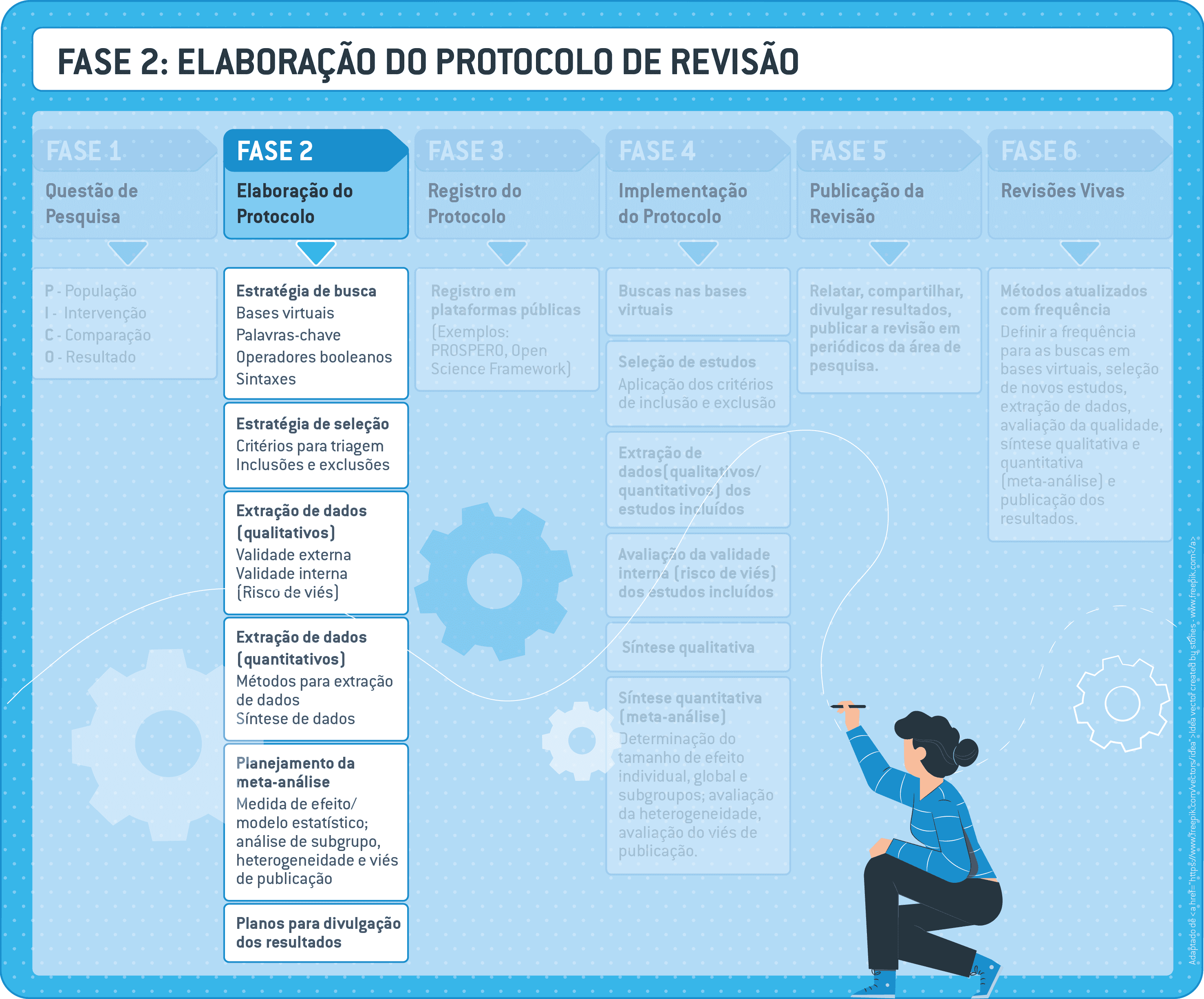
5 Fase 2: elaborando o protocolo de revisão
5.1 Modelos de protocolos
O protocolo é um documento que contém a descrição completa e detalhada de todos os métodos selecionados para responder à pergunta de pesquisa (que foi elaborada na primeira fase do processo).
Diversas organizações especializadas oferecem sugestões de protocolos que seguem boas práticas para revisão sistemática e meta-análise de estudos em geral (PRISMA), em humanos (COCHRANE) ou animais (CAMARADES,SYRCLE).
Sugerimos aqui o uso do formulário estruturado SYRCLE para elaboração de um protocolo completo. O download do formulário na versão .docx pode ser feito AQUI.
Alguns exemplos de protocolos completos de revisão sistemática e meta-análise em Farmacologia podem ser encontrados nas seguintes referências: Ferreira et al., 2022; Martins et al., 2021; Ramos-Hryb et al., 2019 ; Martins et al., 2020
5.2 Planejando a estratégia de busca
O protocolo deve conter um plano detalhado sobre como as publicações relevantes serão obtidas nas bases bibliográficas. Este plano é denominado “estratégia de busca”. *
Uma estratégia de busca consiste na descrição das listas de termos de busca relevantes, também conhecidos como palavras-chave. Estes termos são combinados por operadores booleanos (ex., AND, OR, NOT) e por sintaxes usadas nas pesquisas realizadas em diferentes bancos de dados bibliográficos.
Veja exemplos de estratégia de busca usando termos relacionados a População (P), Intervenção (I) e Desfecho (O) de interesse ou a combinação deles.

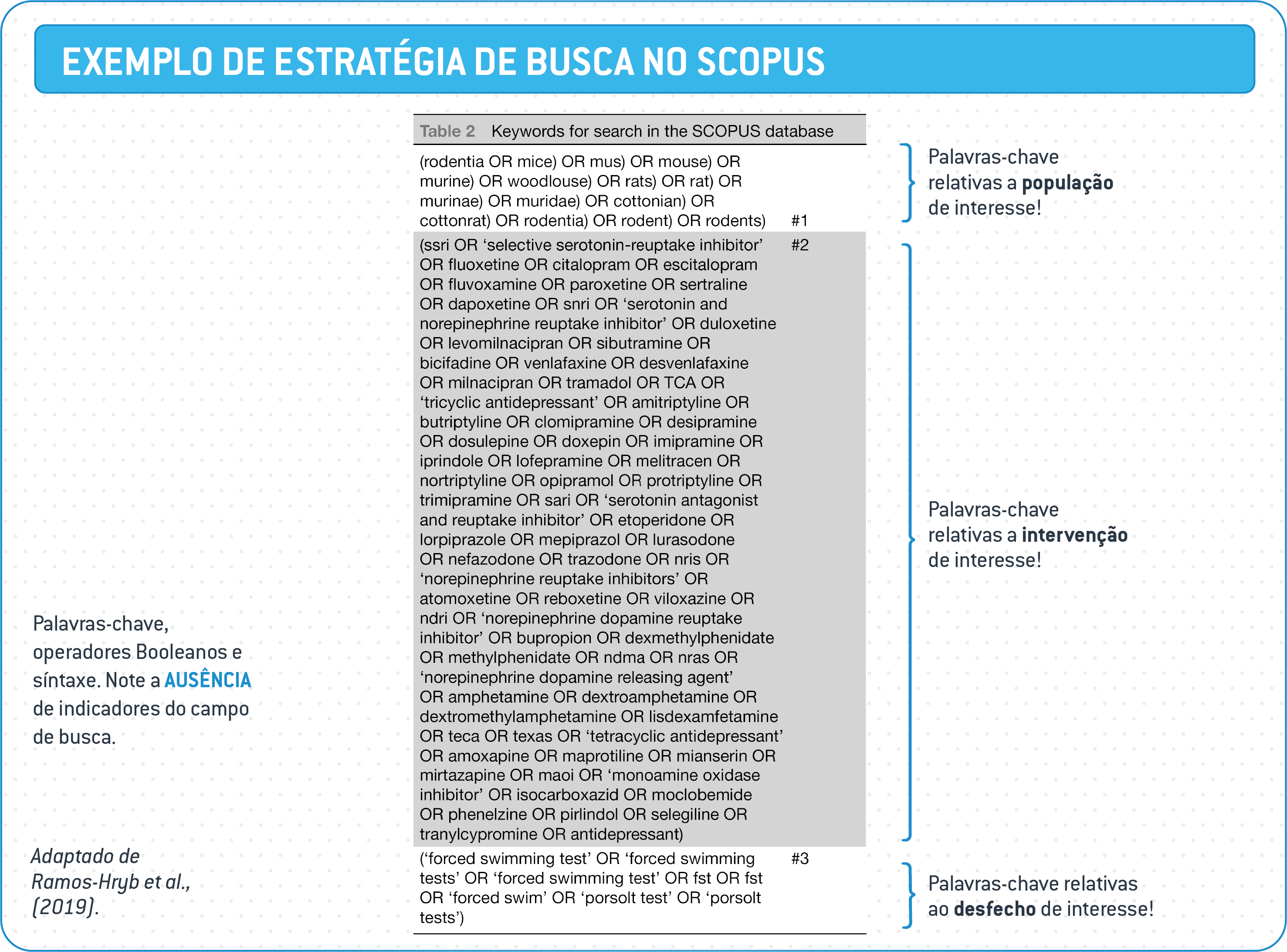
- buscas rápidas, preliminares nas bases bibliográficas, chamadas estudos pilotos, ajudam a estabelecer a estratégia de busca final, a ser apresentada no protocolo;
- os diferentes mecanismos de busca operam de forma diferente. Informe-se sobre estes mecanismos para usá-los de forma adequada;
- em virtude destas diferenças, pesquisas combinando diferentes bases bibliográficas fornecerão uma revisão mais abrangente;
- o acesso a algumas bases bibliográficas requer pagamento ou login institucional.
5.3 Planejando a estratégia de seleção
Neste item, os autores do protocolo deverão descrever como os estudos relevantes serão selecionados entre as publicações recuperadas a partir das bases bibliográficas.
A estratégia de seleção inclui, por exemplo, o planejamento de fases de triagem (pela leitura do título, resumo ou texto completo) e o número de revisores independentes e conciliadores envolvidos. Decisões adicionais podem incluir, por exemplo, entrar em contato com os autores correspondentes no caso de ausência de informações.
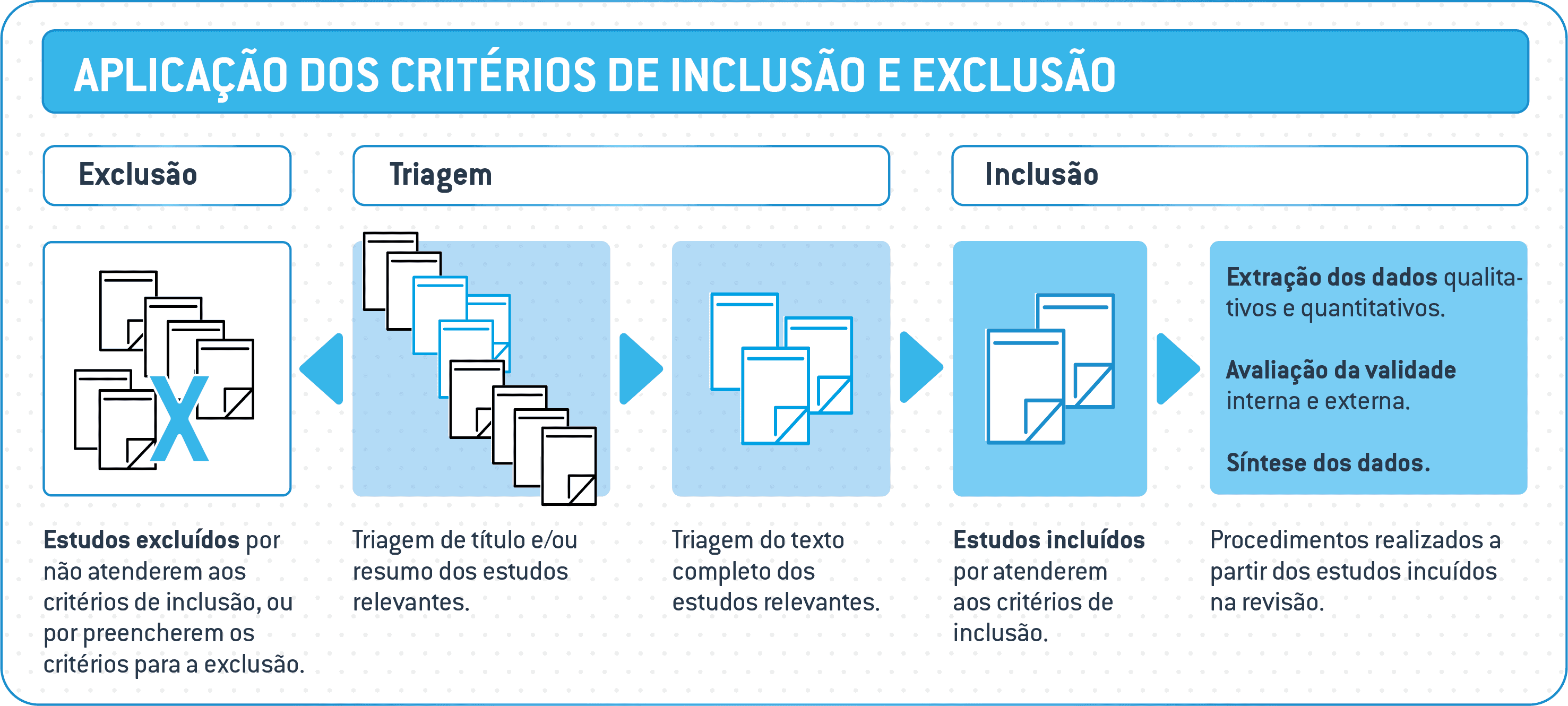
Veja exemplos de protocolos apresentando estratégias de seleção no campo da farmacologia nestas referências: Ballard et al., 2019; Zameer et al., 2019; Pettorruso et al., 2019; David et al., 2019; Sartim et al., 2020
5.4 Planejando a extração de dados
Neste item, os autores do protocolo deverão descrever as abordagens que serão adotadas para extração de dados qualitativos e quantitativos dos estudos incluídos na revisão. Idealmente, essa etapa será realizada por dois revisores independentes, para evitar erros como, por exemplo, a extração de dados incorretos. O protocolo também deve fornecer uma análise de confiabilidade inter-revisores (usando, por exemplo, o índice Kappa de Cohen).
Os dados qualitativos são extraídos para avaliação da validade externa (grau de generalização dos resultados) e validade interna (risco de viés experimental) dos estudos incluídos na revisão.
Para avaliação da validade externa, são extraídas as informações relativas a características dos estudos definidas no momento da elaboração da pergunta usando a ferramenta mnemônica. Por exemplo, se a ferramenta mnemônica aplicada foi a PICO, é possível que você queira extrair e tabular informações sobre a população estudada (ex., espécie, idade e sexo), intervenção farmacológica (ex., tipo de composto, classe do fármaco, a dose, via de administração, duração do tratamento), comparação ou controle (ex., tipo de composto, a via de administração, duração do tratamento) e/ou sobre os desfechos (ex., método de obtenção, tipo de métrica, unidade de medida, análise primária, etc.).
Para avaliação da validade interna, são extraídas as informações requeridas por ferramentas específicas para avaliação do risco de viés. Na Farmacologia, sugerimos o uso das seguintes ferramentas:
- RoB-SYRCLE, adaptada para avaliação de estudos com experimentação animal a partir da ferramenta RoB da Cochrane. No link Ferramentas & Recursos disponibilizamos um guia rápido para o seu uso.
- AMSTAR 2, aplicável para avaliação da qualidade interna das revisões sistemáticas de estudos randomizados ou não randomizados de intervenções em saúde.
Os dados numéricos (ex., médias, desvios-padrão, tamanhos amostrais, número de comparações, valores de p, F ou t, índices de correlação ou qualquer outra medida, manipulação ou transformação dos dados) são necessários para os cálculos de tamanhos de efeito de cada estudo primário e para a condução da meta-análise.
Veja exemplos para avaliação de planejamento da qualidade interna nestas referências: (Ma et al., 2018; Souza et al., 2019; Carabali et al., 2021; Williamson et al., 2016; Azab et al., 2020),
Exemplos de avaliação da qualidade externa de estudos em farmacologia podem ser encontrados em: Lino de Oliveira et al., 2020; Azab et al., 2020; Sartim et al., 2020.
5.5 Planejando a meta-análise
Neste item, os autores do protocolo deverão descrever os planos para calcular o tamanho de efeito de cada estudo individual e da meta-análise.
5.5.1 Cálculos de tamanho de efeito
Os protocolos devem explicar como os tamanhos de efeito serão calculados (ex., diferença média, razão de chances), utilizando dados numéricos extraídos de estudos primários. Além disso, os indicadores da incerteza do tamanho do efeito devem ser mencionados. Geralmente, tamanhos de efeito são apresentados com seus intervalos de confiança.
Tamanhos de efeito são estatísticas usadas para estimar a diferença entre os valores de desfecho (ex., o resultado ou variável dependente) em grupos experimentais (ex., entre o grupo controle e o grupo tratado) ou a força da relação entre um desfecho (ex., resultado ou variável dependente) e uma intervenção (ex., tratamento com um fármaco).
Além do tipo de relação entre variáveis, o tipo de desfecho de interesse (dicotômico ou contínuo, por exemplo) também afeta a escolha do cálculo de tamanho de efeito, a decisão sobre como os tamanhos de efeito estimados nos estudos primários serão combinados e quais serão os indicadores da incerteza do tamanho do efeito combinado (intervalos de confiança, erro padrão, desvio padrão, heterogeneidade).

Legenda: Tabela adaptada de Espírito-Santo e Daniel (2015). M = média de cada grupo; DP = Desvio Padrão de cada grupo; n = número de sujeitos; gl = graus de liberdade (n -1). A tabela é baseada nas seguintes referências: Cohen (1992);Borenstein (2009);Cummings (2012);Hedges (1981);Lakens (2013) e Rosenthal (1994).
No contexto da Farmacologia, o tamanho do efeito poderia ser interpretado como o tamanho do efeito do tratamento com o fármaco sobre a variável estudada.
Num experimento hipotético, farmacologistas poderiam testar a hipótese que a influência do fármaco X sobre uma determinada característica Y de uma amostra de interesse P é maior que a influência do tratamento com o controle C nesta mesma população (“em comparação ao controle C, qual o efeito do fármaco X sobre a medida Y tomada na população P?”).
Neste caso, o cálculo da diferença entre a médias de Y obtidas na amostra P tratada com C ou X, indicaria o tamanho da diferença entre os tratamentos.
Veja exemplos de protocolos de planejamento de tamanhos de efeitos de estudos no campo da Farmacologia em Lino de Oliveira et al., 2020; Carabali et al., 2021; Sartim et al., 2020
5.5.2 Meta-análise
Nesta etapa, os autores do protocolo deverão descrever, para cada desfecho de interesse, se uma meta-análise será conduzida ou não, e como esta decisão será tomada. Além disso, o protocolo deve conter a descrição de como os estudos serão agrupados para calcular o “tamanho do efeito combinado”, qual é o modelo estatístico adequado para combinar os tamanhos de efeito dos estudos primários, quais são os indicadores da incerteza que serão calculados, e como a presença e tamanho de um possível viés de publicação será investigado.
- Meta-análise: sim ou não? O número de estudos disponíveis para o cálculo e que sejam, ao mesmo tempo, semelhantes entre si, é um fator limitante para a meta-análise. Teoricamente, dois estudos semelhantes são suficientes para calcular um tamanho de efeito combinado. Contudo, como acontece com outros métodos estatísticos, uma meta-análise pode fornecer resultados inconclusivos com pequenos tamanhos amostrais. Portanto, cálculos de tamanho amostral ou análise de poder estatístico podem ser feitos, e o protocolo deve conter a descrição destes cálculos.
- Como os estudos serão agrupados para calcular o tamanho do efeito combinado? Cabe aos autores definir, de acordo com a área de pesquisa, quão semelhantes deverão ser os estudos para compor um grupo ou subgrupo de resultados que serão combinados. Exemplos: uma meta-análise será feita com todos os estudos com o mesmo tipo de população (ou intervenção); meta-análises estratificadas serão feitas com estudos agrupados ou categorizados em subgrupos de espécie/linhagem/sexo/idade dos animais experimentais ou de tipos e doses dos fármacos ou de métodos da obtenção do desfecho, etc.
![FIG_13]()
Figura 13. Exemplos de gráficos de floresta feitos a partir de uma meta-análise usando estudos estratificados em subgrupos de população (sexo ou linhagem) ![FIG_14]()
Figura 14. Exemplos de gráficos de floresta feitos a partir de uma meta-análise usando estudos estratificados em subgrupos de intervenção (classe farmacológica ou fármacos) - Modelo estatístico da meta-análise: modelo fixo ou modelos aleatórios? Os estudos primários em Farmacologia, mesmo quando investigam uma mesma hipótese, variam em termos de desenho experimental e nas formas pelas quais os experimentos são conduzidos. Por causa desta heterogeneidade, os modelos de efeitos aleatórios são frequentemente elegíveis para a meta-análise em campos de pesquisa como a Farmacologia.
- Quais indicadores de incerteza das estimativas de tamanho de efeito combinado serão usados? Em geral, cada tamanho de efeito combinado estimado em uma meta-análise ou meta-análise estratificada é acompanhado de intervalos de confiança, erro padrão, desvio padrão e heterogeneidade (ex., estatísticas Q, I²).
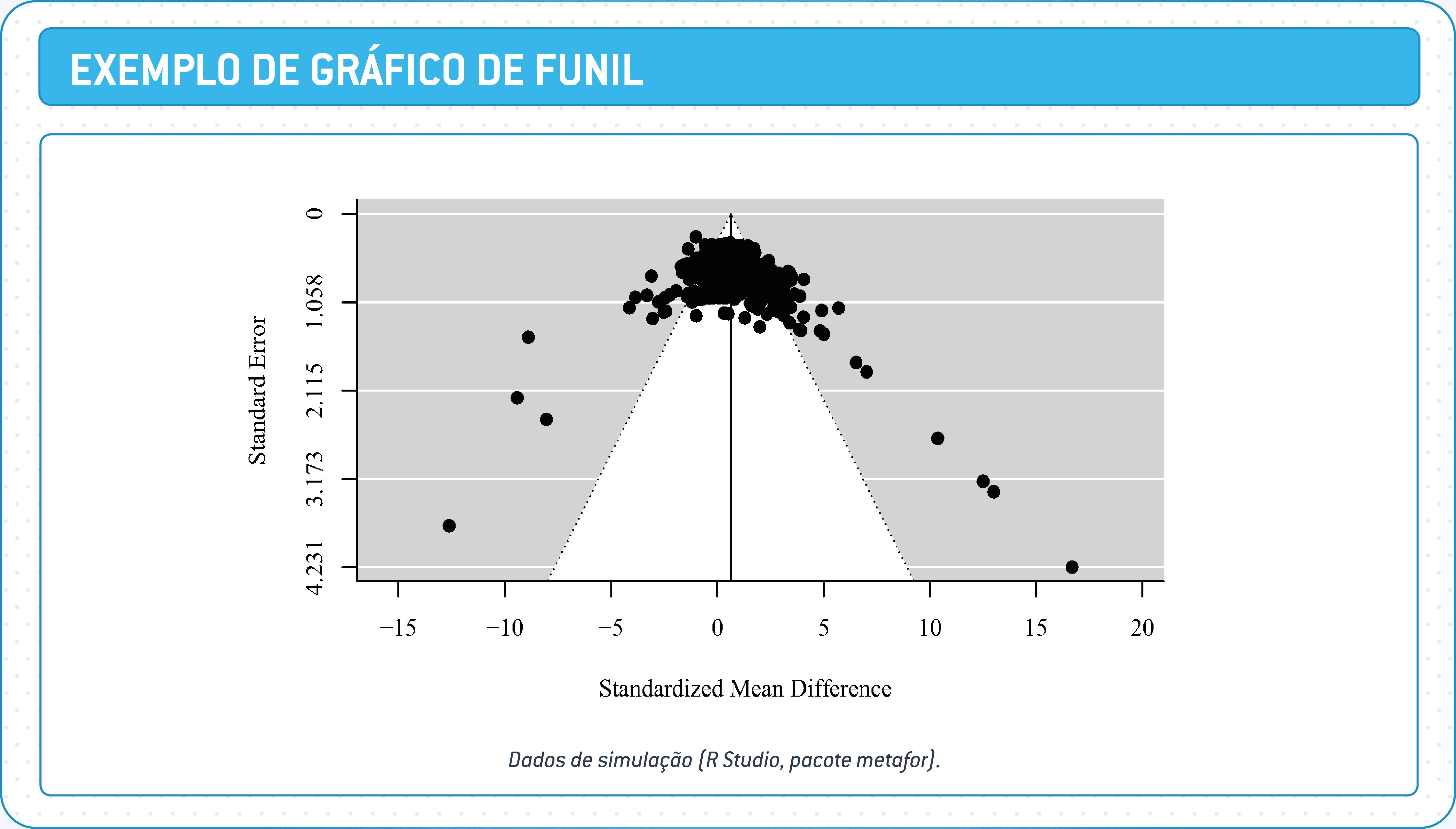
- Como um possível viés de publicação será investigado? O viés de publicação, quando planejado, pode ser avaliado utilizando-se o método de plotagem de funil e trim-and-fill.
![FIG_15]()
Figura 15. Exemplo de gráfico de funil
Veja exemplos de protocolos descrevendo planos para a meta-análise na Farmacologia (Yamato et al., 2014; Soliman et al., 2019; Lino de Oliveira et al., 2020; Carabali et al., 2021; Sartim et al., 2020).
Referências sugeridas: Cochrane Handbook; Sterne et al., (2011); Vesterinen et al., (2014); Borenstein et al., (2009); Shi e Lin, (2019).
5.6 Planejando a publicação dos resultados
Revisões sistemáticas geralmente envolvem diferentes colaboradores e grandes grupos de revisores. Cabe aos autores do protocolo especificar como cada um dos contribuidores receberá o crédito devido e justo por seu aporte, para acomodar as expectativas de todos os envolvidos. Também cabe a eles identificar os meios de comunicação adequados para disponibilizar os resultados ao público.
Veja exemplos de protocolos descrevendo planos de disseminação no campo da farmacologia em (Kavanagh et al., 2019; Lee et al., 2019)
5.7 Planejando a revisão sistemática viva
Finalmente, os farmacologistas poderão manter suas revisões sistemáticas e meta-análises vivas.
A Colaboração Cochrane disponibiliza orientações para o delineamento dos métodos, produção e publicação de revisões sistemáticas vivas nas áreas clínicas, no Cochrane Database of Systematic Reviews.
- A CAMARADES BR oferece aqui uma proposta de formulário, adaptado da Colaboração Cochrane, para revisões sistemáticas e meta-análises vivas em Farmacologia. Faça o download AQUI.
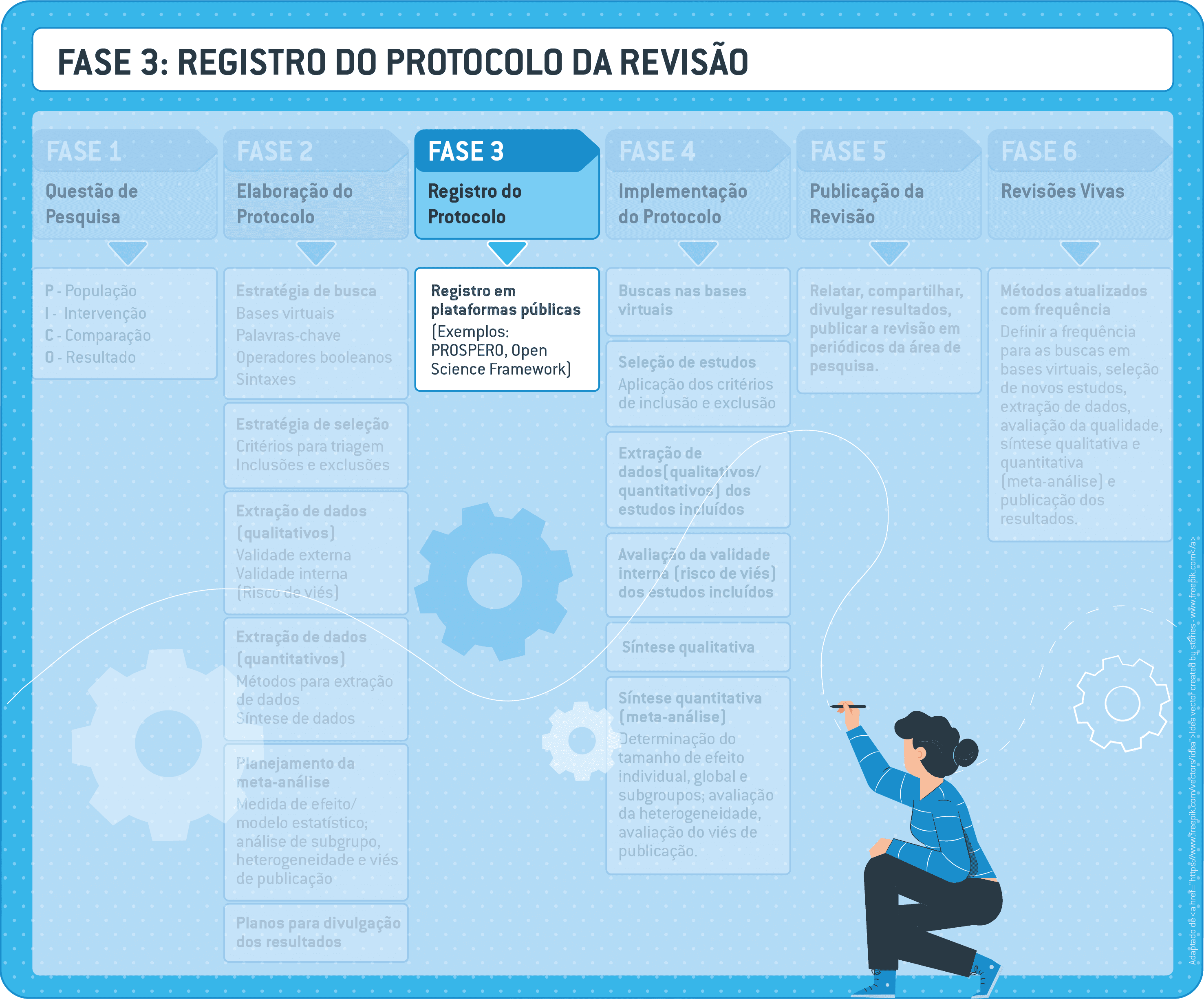
6 Fase 3: registrando o protocolo de revisão
6.1 Plataformas públicas de registro
O registro do protocolo, feito antes de realizar a revisão sistemática e meta-Análise, pode ajudar os revisores a aderirem ao plano e reduz a incidência de revisões tendenciosas, uma vez que uma longa lista de decisões precisa ser tomada sobre o processo. Pode ser necessário voltar ao protocolo em qualquer estágio da revisão, para encontrar informações necessárias para implementação das suas atividades.
Farmacologistas podem registrar suas revisões em plataformas públicas, como:
- PROSPERO: plataforma especializada em registros de protocolos para Revisões Sistemáticas e Meta-Análises de estudos relevantes para a saúde humana em humanos ou animais de laboratório;
- Open Science Framework: plataforma pública e gratuita usada para depositar protocolos científicos de qualquer estudo, incluindo protocolos de revisão sistemática e meta-análise.
NOTA: os registros também podem ser feitos em revistas científicas de revisão por pares. Veja exemplos em Soliman et al., 2019; Lee et al., 2019; Kavanagh et al., 2019;Ramos-Hryb et al., 2019; Ang et al., 2020; Maguire and Guérin, 2020, Thombs et al., 2020 , Bolzan e Lino de Oliveira, 2021.
Fase 4: implementação do protocolo de revisão
A implementação do protocolo de revisão (fase 4) consiste em colocar em prática as ações previstas no protocolo previamente elaborado (fase 2) e registrado (fase 3).
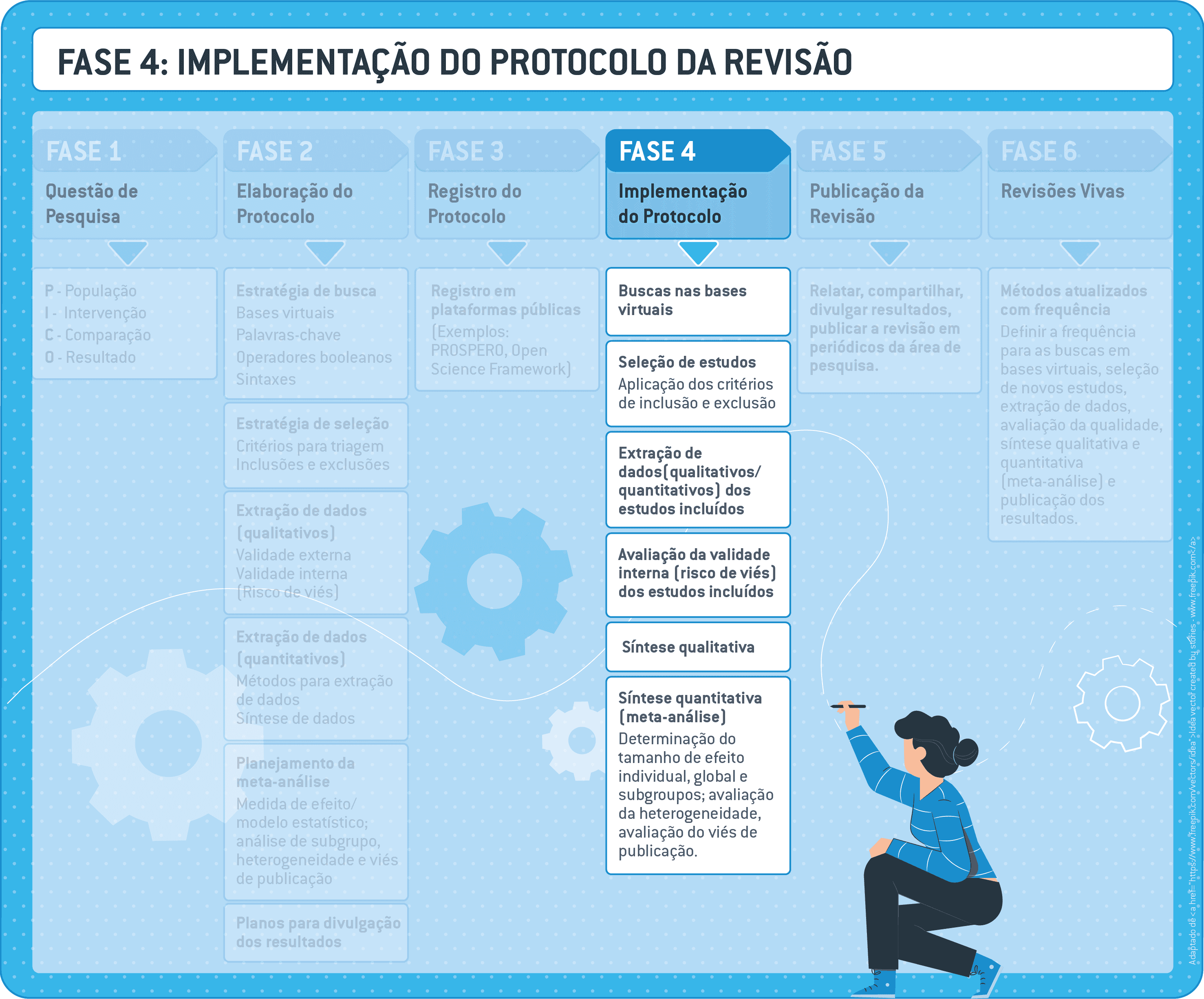
Ao longo do processo de implementação, os revisores precisam fazer anotações completas sobre todas as decisões tomadas nesta fase, incluindo os eventuais desvios em relação ao descrito no protocolo.
Estas anotações aumentam a transparência e ajudam a organizar o trabalho da equipe. Além disso, ajudam os leitores a julgar a qualidade da revisão.
7.1 Softwares, scripts e outros recursos gratuitos
Identificamos diversos recursos, gratuitos ou comerciais, disponíveis para implementar os processos de uma revisão sistemática e meta-análise e que podem beneficiar revisões em temas farmacológicos. Os níveis de automatização destas ferramentas variam, mas, no geral, aceleram as atividades necessárias para a revisão.
Veja abaixo exemplos de ferramentas úteis e, em sua maioria, gratuitas.
7.1.1 Busca em bases bibliográficas
O menu de "pesquisa avançada" dos buscadores de bases bibliográficas virtuais (por exemplo, Medline via Pubmed, Scopus,Web of Science, Embase) costuma ser mais apropriado para o tipo de pesquisa necessária em uma revisão sistemática do que o menu de busca simples.
Recuperar documentos de diferentes bases virtuais requer auxílio de um software de gerenciamento de referência para deduplicação. O Mendeley, Zotero, e Rayyan são exemplos de gerenciadores grátis. A CAMARADES desenvolveu um aplicativo web para Gdeduplicação Automated Systematic Search Deduplication Tool (ASySD).
O número de publicações obtidas nas pesquisas realizadas em cada uma das bases bibliográficas, antes e depois da deduplicação, deve ser anotado em um fluxograma PRISMA que será apresentado no relatório final da revisão. O fluxograma PRISMA pode ser baixadoAQUI.
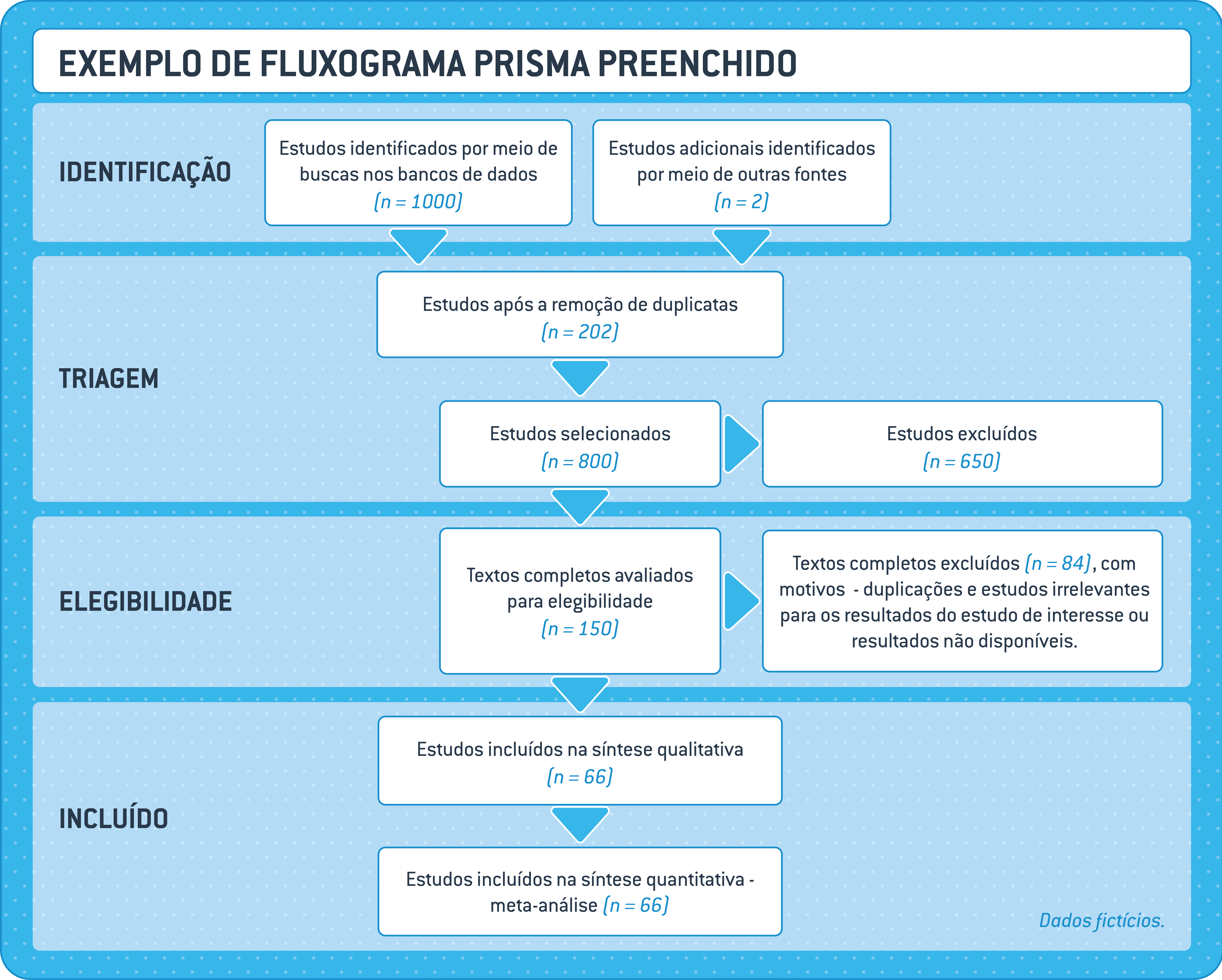
7.1.2 Triagem de estudos relevantes
O software de gerenciamento de referência também é útil para aplicar os critérios de seleção e elegibilidade de estudos relevantes. Por exemplo: Mendeley e Rayyan podem ser usados para classificar semi-automaticamente as referências em uma biblioteca.
Outros recursos gratuitos são ASReview, Parsifal, Rvtools (ferramentas para síntese de evidências em R), Sysrev, Screenatron e Systematic Review Accelerator e SyRF (CAMARADES).
Os resultados dos processos de triagem (número de estudos excluídos, motivos de exclusão, número de estudos incluídos) devem ser anotados em um fluxograma PRISMA que será apresentado no relatório final da revisão. O fluxograma PRISMA pode ser baixado AQUI.
7.1.3 Extração de dados
Gerenciadores de referências (Mendeley, Zotero e Rayyan) podem ser úteis para obter informações bibliográficas dos estudos incluídos (por exemplo, nome dos autores, ano, revista).
Ferramentas online, como Colandr e o SyRF, ajudam a anotar, tabular, compartilhar e gerenciar dados qualitativos e numéricos extraídos das publicações de forma eficiente. Existem versões gratuitas de ferramentas como a Engauge Digitizer ou WebPlotDigitizer que convertem imagens de gráficos ou mapas em números. Medições manuais de elementos de gráficos (escala ou tamanhos de barras ou extensões de linhas e outros atributos) são possíveis usando a régua digital de leitores de PDF (por exemplo, versão gratuita do Adobe Acrobat Reader DC).
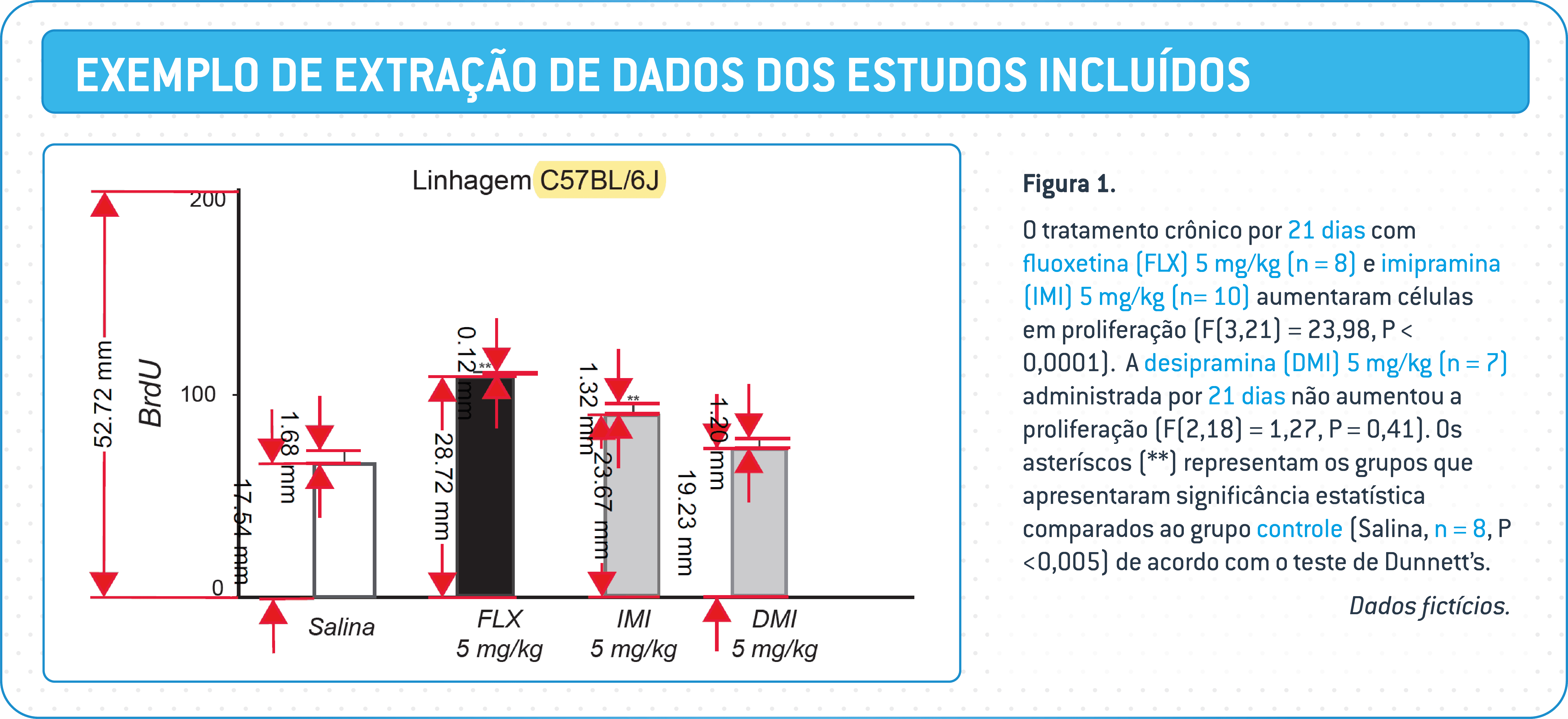
Algum conhecimento de linguagem de programação permite usar o pacote de metaDigitise R emetagearpara extrair estatísticas descritivas. Tabelas em formato .csv podem ser formatadas para uso em futuras meta-análises (Tabela 1).
O pacote pacman é uma ferramenta de gerenciamento de pacotes R, que combina funcionalidades dplyr, irr, e rel, usados para cálculos de concordâncias entre revisores ( Cohen Kappa), sempre que dois revisores independentes realizarem uma atividade. Disponibilizamos aqui no SysPhar modelos de tabela .csv para análises de concordâncias entre revisores (Tabela 2) além de scripts para o uso da ferramenta Pacman.
7.1.4 Avaliação do risco de viés usando a ferramenta RoB-Syrcle
A apresentação dos dados da ferramenta RoB-Syrcle pode ser facilitada por ferramenta robvis (veja McGuinness and Higgins, 2020). Disponibilizamos aqui no SysPhar modelos de tabela .csv para avaliação do risco de viés (Tabela 3) e de scripts para o uso da ferramenta Robvis.
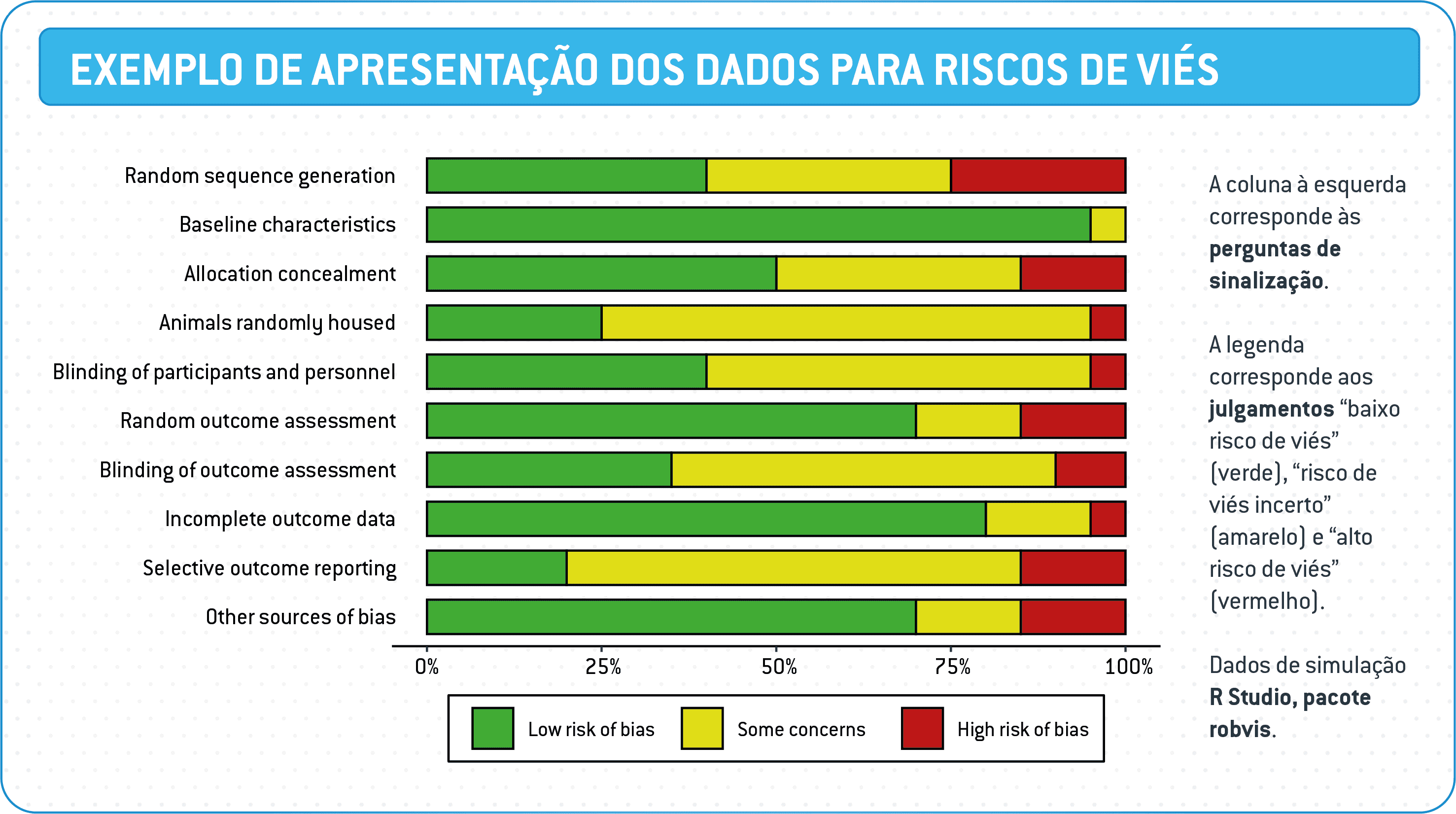
7.1.5 Cálculo de meta-análise
Ferramentas como Meta-Meta-essentials,RevManou OpenMEE podem ser usadas gratuitamente na condução da meta-análise por revisores não familiarizados com softwares estatísticos ou linguagens de programação.
Os revisores familiarizados com a codificação podem se beneficiar de softwares como pacotes e scripts Meta ou Metafor em R, Python ou OpenMeta [Analista]. O pacote metagear para o R é um recurso gratuito que, além de facilitar a triagem e a extração de dados, também é usado para meta-análise.
Disponibilizamos aqui no SysPhar modelos de scripts para o metafor (meta-análise, viés de publicação) além do metapower para cálculo do poder estatístico, se aplicável.
8 Fase 5: publicação dos resultados da revisão
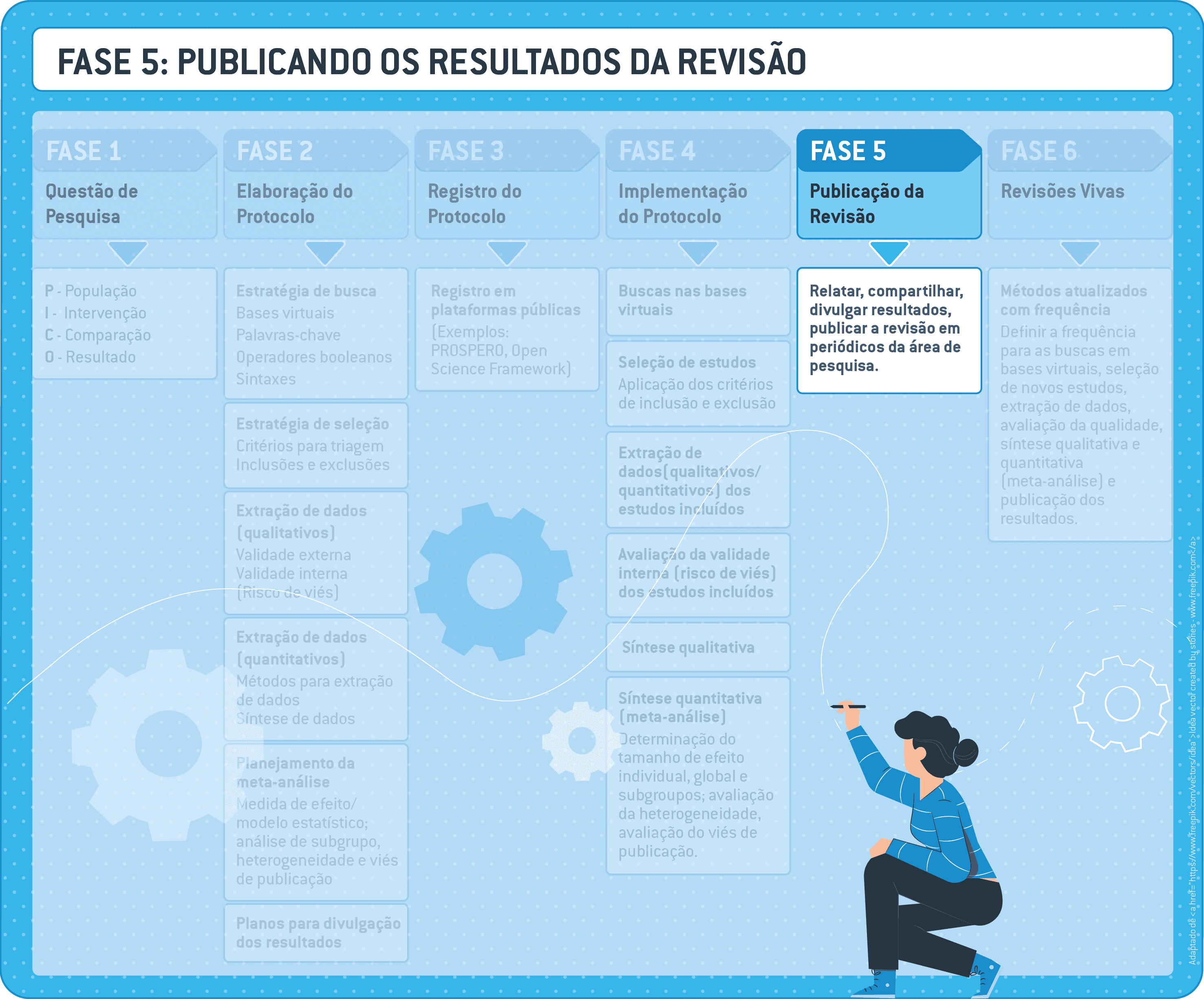
8.1 Onde e como publicar?
Existem diferentes estratégias para publicar, compartilhar e divulgar resultados da revisão, incluindo eventos científicos, workshops ou plataformas online e revistas nas quais as publicações são revisadas por pares.
Em periódicos com revisão por pares, salvo algumas especificações, o relatório da revisão sistemática e meta-análise pode ser organizado como em outros tipos de publicações. Alguns periódicos solicitam que os artigos enviem uma lista de verificação PRISMA, para facilitar o processo de revisão por pares.
A publicação pode ser organizada da seguinte forma:
- introdução: histórico teórico, hipótese e questão de revisão;
- métodos: brevemente apresentados, incluindo o número de registro do protocolo, estratégia de pesquisa, estratégia de triagem, extração de dados, avaliações de qualidade e análise. É importante que cálculos e interpretações de tamanhos de efeito devem ser explicitamente declarados, porque têm impacto na discussão dos dados;
- resultados: descrição dos resultados dos processos de busca e triagem de estudos, apresentando:
- o fluxograma PRISMA como figura do artigo;
- a descrição das qualidades das publicações incluídas na revisão e sistematização dos resultados em tabelas, para a discussão da validade externa dos estudos);
- os resultados da análise de risco de viés dos estudos incluídos na revisão, para a discussão da validade interna dos estudos;
- os resultados numéricos da meta-análise (estimativas de tamanho de efeito combinado global com ou sem correção pelo viés de publicação, estimativas de tamanho de efeito combinado estratificados por subgrupos, heterogeneidade das estimativas);
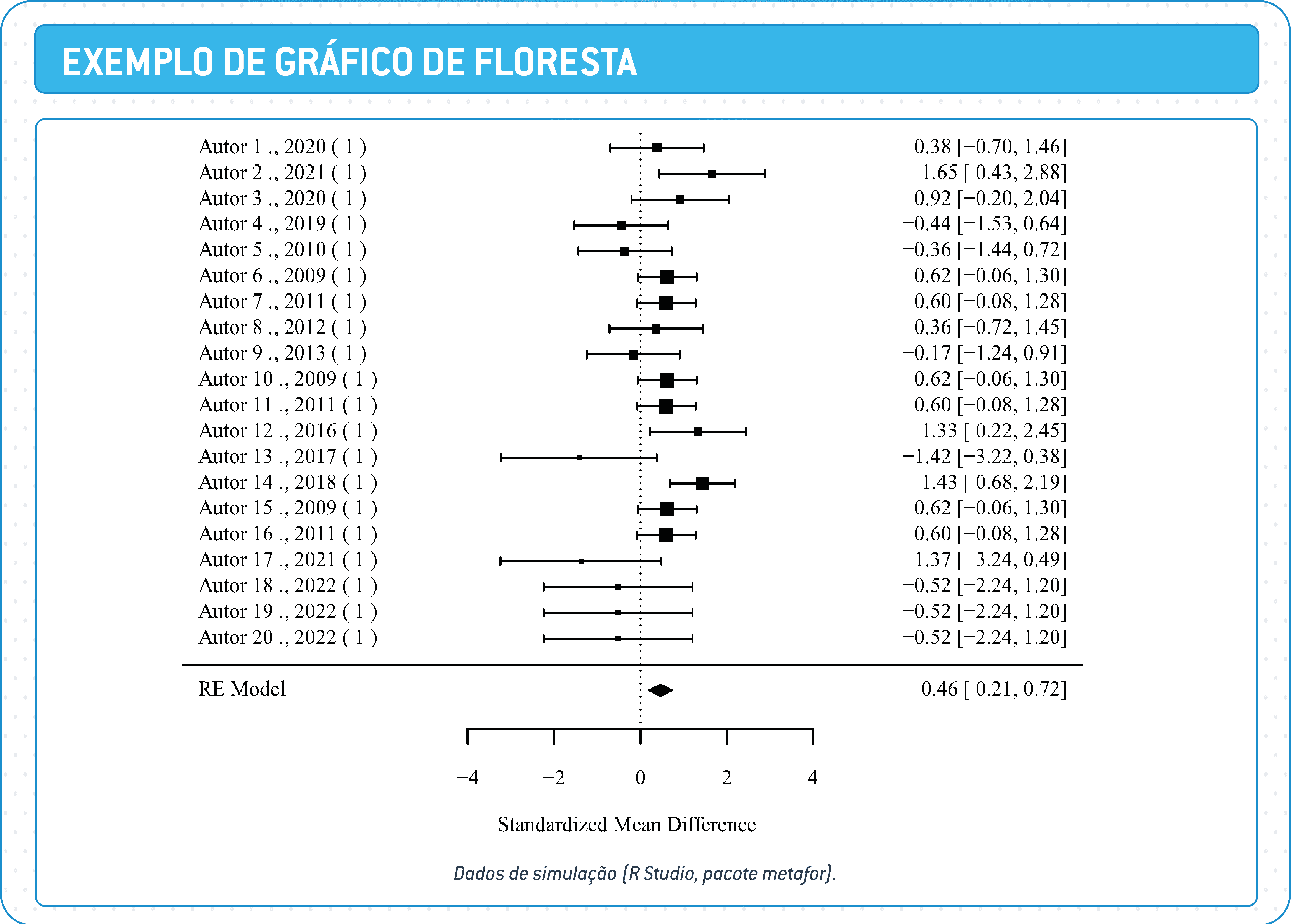
- E a apresentação gráfica, para a qual em geral se usa o gráfico de floresta para meta-análise e gráficos de funil quando a avaliação do viés de publicação for realizada.
- Discussão, na qual devem ser abordados:
- avaliação da qualidade interna e externa das publicações incluídas;
- os resultados da meta-análise (direção, magnitude e heterogeneidade das estimativas de efeito combinado);
- o impacto da qualidade dos estudos, do risco de vieses experimentais, do risco de viés de publicação e da heterogeneidade dos estudos sobre as estimativas de tamanho do efeito combinado.
- conclusão: deve incluir a confiabilidade dos resultados da revisão de acordo com as avaliações da qualidade, heterogeneidade, viés de publicação. As limitações do processo de revisão podem ser divulgadas.
9 Fase 6: mantendo a revisão sistemática viva
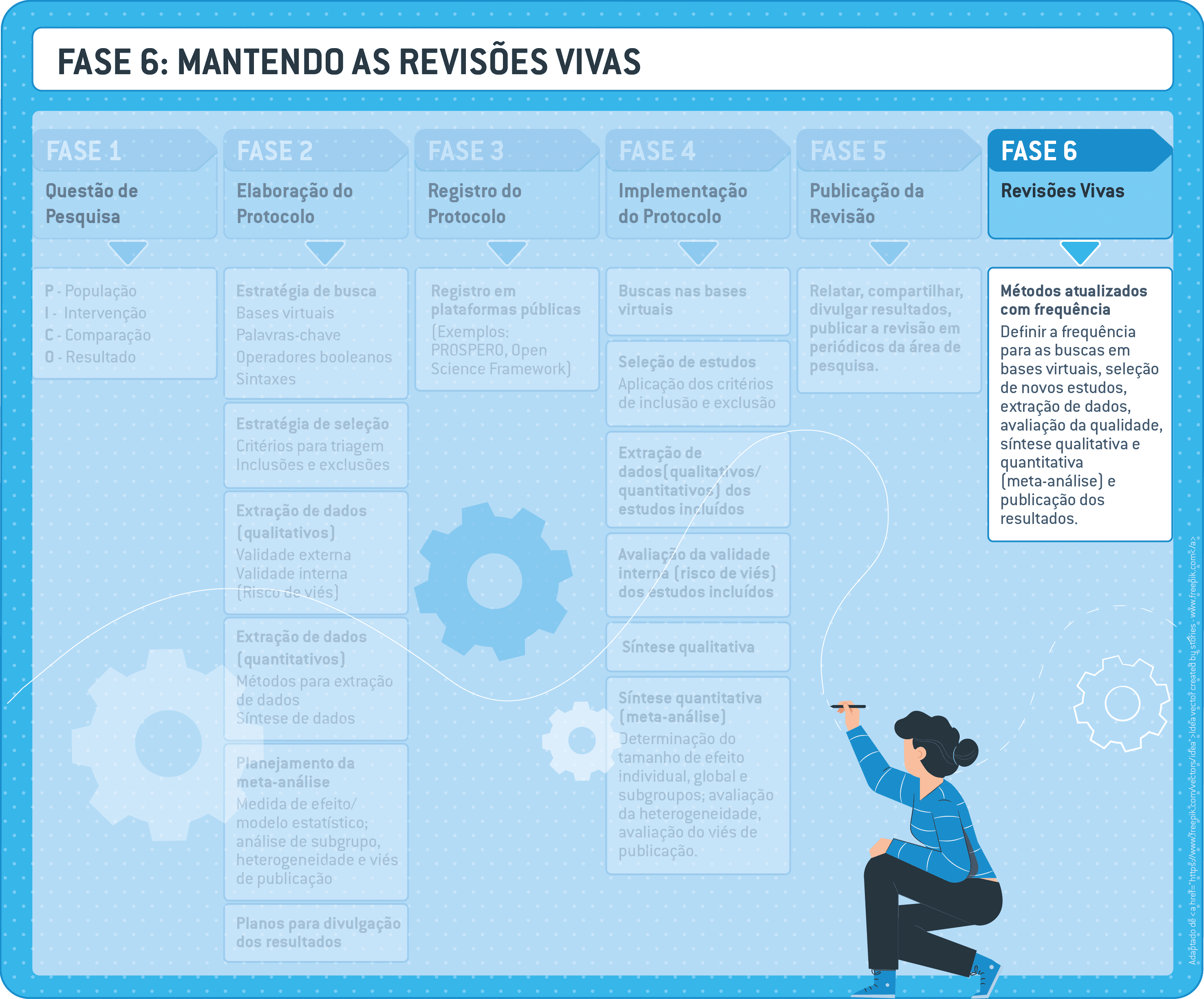
9.1 Atualização da revisão sistemática
As diretrizes existentes até ao momento (fevereiro de 2022) orientam que revisões sistemáticas vivas sejam publicadas de acordo com modelos semelhantes às publicações Cochrane.
Os modelos disponíveis são os seguintes:
- nova publicação a cada nova atualização (geralmente feita em intervalos anuais), obtendo uma nova versão e DOI no PubMed;
- publicação em que a introdução e os métodos do manuscrito principal não são alterados, apenas a seção de resultados. Obs.: o manuscrito exigirá menos recursos para preparar no segundo modelo, mas a versão original deve ter sido escrita de maneira genérica para acomodar novas informações emergentes em versões subsequentes;
- publicação em que as descobertas das análises atualizadas possam ser apresentadas como novos apêndices, sem alteração no resumo ou manuscrito original. Obs.: esse modelo torna difícil adicionar ou remover autores de acordo com as mudanças em sua contribuição para as versões subsequentes;
- ou um modelo em que os resultados das atualizações são resumidos em repositórios de dados de domínio público, que apresentam os resultados atualizados visualmente. Obs.: idealmente, esses repositórios devem ser interativos (por exemplo: aplicativo RShiny).
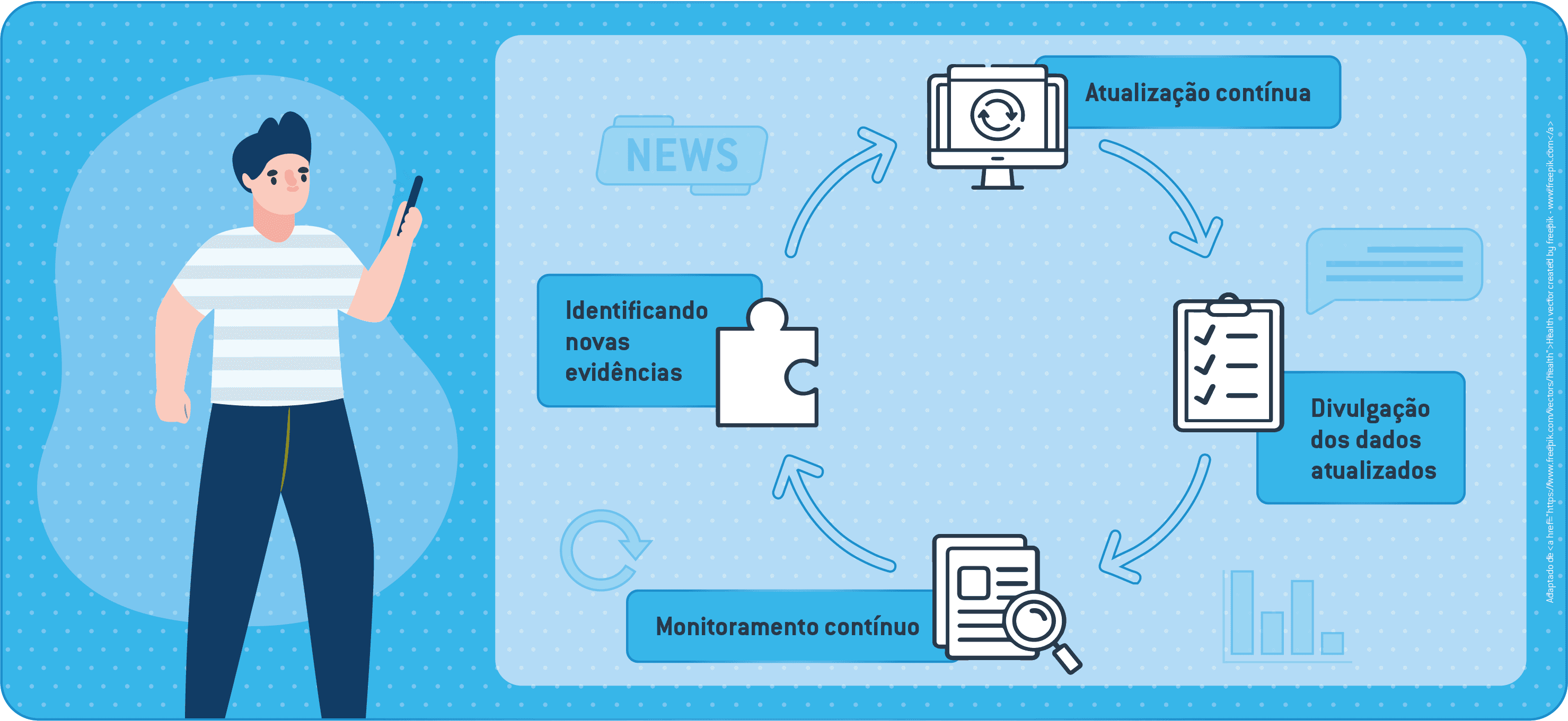
Quando nenhum estudo novo é identificado para a inclusão, apenas a data de pesquisa publicada precisa ser atualizada. Se novos estudos forem identificados, é necessária uma nova publicação.
10 Sobre
10.1 SysPhar
SysPhar (do inglês Systematic Pharmacology) é um recurso produzido e oferecido gratuitamente pela CAMARADES BR cujo desenvolvimento foi apoiado pela fundação Alexander von Humboldt.
Neste guia SysPhar, reunimos e organizamos informações, documentos, links e outras ferramentas que consideramos úteis para ajudar farmacologistas a fazerem suas revisões sistemáticas e meta-análises em Farmacologia.
Os recursos apresentados no SysPhar estão publicamente disponíveis nas páginas de organizações como a CAMARADES, Cochrane, OSF, PROSPERO, SYRCLE, PRISMA e outros. Agradecemos a essas organizações e equipes por disponibilizarem esses recursos pública e gratuitamente!
Este recurso foi atualizado pela última vez em: 07 de Agosto de 2023.
10.2 Como citar a ferramenta?
SysPhar. Systematic Pharmacology, (Janeiro de 2022), CAMARADES Brasil. Disponível em https://camaradesbrasil.bio.br/. Acessado em 11 de ago. de 2023.
10.3 Nossa equipe
Versão em português e inglês:
- Juliana Aparecida Bolzan, MSc.
- Cilene Lino de Oliveira, PhD.
- Tamires Martins, MSc.
- Sofia Diehl Döring, PharmB.
10.4 Apoiadores
10.5 Contato
Se você tiver dúvidas sobre os recursos, quiser fazer uma pergunta específica ou contribuir para o texto, entre em contato conosco aqui